Struktur, sifat, tata nama, penggunaan perak sulfida (Ag2S)
itu perak sulfida adalah senyawa anorganik yang rumus kimianya adalah Ag2S. Terdiri dari padatan hitam keabu-abuan yang dibentuk oleh kation Ag+ dan anion S2- dalam rasio 2: 1. S2- ini sangat mirip dengan Ag+, karena keduanya adalah ion lunak dan mereka berhasil saling menstabilkan.
Ornamen perak cenderung gelap, kehilangan kilau karakteristik mereka. Perubahan warna bukanlah produk dari oksidasi perak, tetapi dari reaksinya dengan hidrogen sulfida yang ada di lingkungan pada konsentrasi rendah; Ini bisa berasal dari pembusukan atau degradasi tanaman, hewan atau makanan yang kaya akan sulfur.

H2S, yang molekulnya membawa atom belerang, bereaksi dengan perak sesuai dengan persamaan kimia berikut: 2Ag (s) + H2S (g) => Ag2S + H2(g)
Oleh karena itu, Ag2S bertanggung jawab atas lapisan hitam yang terbentuk pada perak. Namun, di alam belerang ini juga dapat ditemukan di mineral acantita dan argentita. Kedua mineral tersebut dibedakan dari banyak mineral lainnya dengan kristal hitam dan cerahnya, seperti halnya padatan pada gambar atas.
Ag2S menghadirkan struktur polimorfik, sifat elektronik dan optoelektronik yang menarik, adalah semikonduktor dan menjanjikan bahan untuk pengembangan perangkat fotovoltaik, seperti sel surya.
Indeks
- 1 Struktur
- 2 Properti
- 2.1 Berat molekul
- 2.2 Penampilan
- 2.3 Bau
- 2.4 Titik lebur
- 2.5 Kelarutan
- 2.6 Struktur
- 2.7 Indeks bias
- 2.8 Konstanta dielektrik
- 2.9 Elektronik
- 2.10 Reaksi reduksi
- 3 Nomenklatur
- 3.1 Sistematika
- 3.2 Stok
- 3.3 Tradisional
- 4 Penggunaan
- 5 Referensi
Struktur
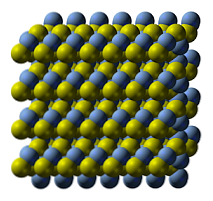
Struktur kristal perak sulfida diilustrasikan pada gambar atas. Bola biru sesuai dengan kation Ag+, sedangkan yang kuning ke anion S2-. Ag2S adalah polimorfik, yang berarti dapat mengadopsi beberapa sistem kristal pada kondisi suhu tertentu.
Bagaimana? Melalui fase transisi. Ion-ion disusun ulang sedemikian rupa sehingga kenaikan suhu dan getaran padatan tidak mengganggu kesetimbangan tarik-tolakan elektrostatik. Ketika ini terjadi dikatakan bahwa ada transisi fase, dan padat karena itu menunjukkan sifat fisik baru (seperti kilau dan warna).
Ag2S pada suhu normal (lebih rendah dari 179ºC), ia memiliki struktur kristal monoklinik (α-Ag2S). Selain fase padat ini ada dua lainnya: bcc (kubik berpusat di tubuh) antara 179 hingga 586ºC, dan fcc (kubik berpusat di wajah) pada suhu yang sangat tinggi (Ag-Ag2S).
Mineral argentit terdiri dari fase fcc, juga dikenal sebagai β-Ag2S. Setelah didinginkan dan diubah menjadi tebing, fitur struktural mereka menang dikombinasikan. Oleh karena itu, kedua struktur kristal tersebut hidup berdampingan: monoklinik dan bcc. Oleh karena itu, padatan hitam dengan warna cerah dan menarik muncul.
Properti
Berat molekul
247,80 g / mol
Penampilan
Kristal hitam keabu-abuan
Bau
Toilet.
Titik lebur
836ºC. Nilai ini setuju dengan fakta bahwa Ag2S adalah senyawa dengan sedikit karakter ionik dan karenanya meleleh pada suhu di bawah 1000ºC.
Kelarutan
Dalam air hanya 6,21 ∙ 10-15 g / L pada 25ºC. Artinya, jumlah padatan hitam yang dilarutkan dapat diabaikan. Ini, sekali lagi, disebabkan oleh karakter polar kecil dari ikatan Ag-S, di mana tidak ada perbedaan signifikan keelektronegatifan antara kedua atom.
Juga, Ag2S tidak larut dalam semua pelarut. Tidak ada molekul yang dapat secara efisien memisahkan lapisan kristalnya dalam ion Ag+ dan S2- dipecahkan.
Struktur
Empat lapisan ikatan S-Ag-S juga dapat dilihat pada gambar struktur, yang bergerak satu sama lain ketika benda padat mengalami pemahaman. Perilaku ini berarti bahwa, walaupun merupakan semikonduktor, ia bersifat ulet seperti banyak logam pada suhu kamar.
Lapisan S-Ag-S cocok dengan baik karena geometri sudutnya yang diamati sebagai zigzag. Memiliki kekuatan pemahaman, ini bergerak pada sumbu perpindahan sehingga menyebabkan interaksi non-kovalen baru antara atom perak dan belerang.
Indeks bias
2.2
Konstanta dielektrik
6
Elektronik
Ag2S adalah semikonduktor amfoter, yaitu, berperilaku seolah-olah itu adalah tipe n dan dari jenisnya hal. Itu juga tidak rapuh, sehingga telah dipelajari untuk penerapannya dalam perangkat elektronik.
Reaksi reduksi
Ag2S dapat direduksi menjadi perak logam dengan memandikan potongan-potongan hitam dengan air panas, NaOH, aluminium dan garam. Reaksi berikut terjadi:
3Ag2S + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2O3(s)
Nomenklatur
Silver, yang konfigurasi elektroniknya [Kr] 4d105s1, ia hanya dapat kehilangan satu elektron: elektron 5s yang paling luar. Demikianlah, Agation+ tetap dengan konfigurasi elektronik [Kr] 4d10. Oleh karena itu, ia memiliki valensi unik +1, yang menentukan bagaimana senyawanya harus disebut.
Belerang, di sisi lain, memiliki konfigurasi elektronik [Ne] 3s23p4, dan itu membutuhkan dua elektron untuk menyelesaikan oktet valensi. Ketika memperoleh dua elektron ini (dari perak), ia berubah menjadi anion belerang, S2-, dengan konfigurasi [Ar]. Artinya, isoelektronik untuk argon gas mulia.
Jadi Ag2S harus dipanggil sesuai dengan nomenklatur berikut:
Sistematika
Monyetbelerang diperak Di sini kita mempertimbangkan jumlah atom dari setiap elemen dan ditunjukkan oleh awalan pembilang Yunani.
Stok
Perak sulfida. Ketika memiliki valensi unik +1, itu tidak ditentukan dengan angka Romawi dalam tanda kurung: silver sulfide (I); yang salah.
Tradisional
Sulfuro argéntico. Karena perak "bekerja" dengan valensi +1, akhiran -ico ditambahkan ke namanya argentum dalam bahasa Latin.
Penggunaan
Beberapa kegunaan baru untuk Ag2S adalah yang berikut:
-Solusi pewarnaan nanopartikel mereka (dengan ukuran yang berbeda), memiliki aktivitas antibakteri, tidak beracun, dan karenanya dapat digunakan dalam bidang kedokteran dan biologi.
-Partikelnano mereka dapat membentuk apa yang dikenal sebagai titik kuantum. Ini menyerap dan memancarkan radiasi dengan intensitas lebih besar daripada banyak molekul neon organik, sehingga mereka dapat menggantikan yang terakhir sebagai penanda biologis.
-Struktur α-Ag2S membuatnya menunjukkan sifat elektronik yang mencolok untuk digunakan sebagai sel surya. Ini juga merupakan titik awal untuk sintesis bahan dan sensor termoelektrik baru.
Referensi
- Mark Peplow. (17 April 2018). Semikonduktor perak sulfida membentang seperti logam. Diambil dari: cen.acs.org
- Kolaborasi: Penulis dan editor struktur kristal volume III / 17E-17F-41C () Perak sulfida (Ag2S). Dalam: Madelung O., Rössler U., Schulz M. (eds) Unsur-Unsur Berikat Non-Tetrahedral dan Senyawa Biner I. Landolt-Börnstein - Kelompok III Materi Terkondensasi (Data Angka dan Hubungan Fungsional dalam Sains dan Teknologi), vol 41C. Springer, Berlin, Heidelberg.
- Wikipedia. (2018). Perak sulfida. Diambil dari: en.wikipedia.org
- Stanislav I. Sadovnikov & col. (Juli 2016). Ag2Nanopartikel perak sulfida dan larutan koloid: Sintesis dan sifat. Diambil dari: sciencedirect.com
- Bahan Azo. (2018). Silver Sulfide (Ag2S) Semikonduktor. Diambil dari: azom.com
- A. Nwofe. (2015). Prospek dan tantangan film tipis perak sulfida: Tinjauan. Divisi Ilmu Bahan & Energi Terbarukan, Departemen Fisika Industri, Universitas Negeri Ebonyi, Abakaliki, Nigeria.
- UMassAmherst. (2011). Demonstrasi Kuliah: membersihkan perak yang ternoda. Diambil dari: lecturedemos.chem.umass.edu
- Belajar. (2018). Apa itu Silver Sulfide? - Formula & Penggunaan Kimia. Diambil dari: study.com


