Properti, Struktur, Penggunaan dan Risiko Tin Chloride (SnCl2)
itu timah klorida (II) atau stannous chloride, dari rumus kimia SnCl2, adalah senyawa padat kristal putih, produk dari reaksi timah dan larutan asam klorida pekat: Sn (s) + 2HCl (conc) => SnCl2(aq) + H2(g) Proses sintesis (persiapan) terdiri dari menambahkan potongan pengajuan timah untuk bereaksi dengan asam.
Setelah menambahkan potongan-potongan timah, itu melanjutkan untuk melakukan dehidrasi dan kristalisasi sampai garam anorganik diperoleh. Dalam senyawa ini, timah telah kehilangan dua elektron dari kulit valensinya untuk membentuk ikatan dengan atom klor.
Ini dapat lebih dipahami jika seseorang mempertimbangkan konfigurasi valensi timah (5s25 px2haldan0halz0), dimana pasangan elektron menempati orbital px diberikan kepada proton H+, untuk membentuk molekul hidrogen diatomik. Yaitu, ini adalah reaksi tipe redoks.
Indeks
- 1 Sifat fisik dan kimia
- 1.1 konfigurasi Valencia
- 1.2 Reaktivitas
- 1.3 Aktivitas reduktif
- 2 struktur kimia
- 3 Penggunaan
- 4 Risiko
- 5 Referensi
Sifat fisik dan kimia
Tautan SnCl2 Apakah mereka ionik atau kovalen? Sifat fisik timah (II) klorida mengesampingkan opsi pertama. Titik lebur dan titik didih untuk senyawa ini adalah 247 ° C dan 623 ° C, menunjukkan interaksi intermolekul yang lemah, fakta umum untuk senyawa kovalen.
Kristalnya berwarna putih, yang diterjemahkan ke dalam nol penyerapan dalam spektrum yang terlihat.
Konfigurasi Valencia
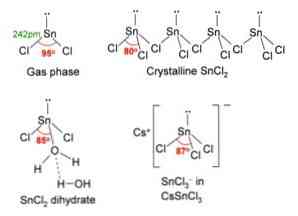
Pada gambar di atas, di sudut kiri atas, molekul SnCl terisolasi diilustrasikan2.
Geometri molekul harus rata karena hibridisasi atom pusat adalah sp2 (3 orbital sp2 dan orbital p murni untuk membentuk ikatan kovalen), tetapi pasangan elektron bebas menempati volume dan menekan atom klor ke bawah, memberikan molekul geometri sudut.
Dalam fase gas senyawa ini diisolasi, sehingga tidak berinteraksi dengan molekul lain.
Seperti hilangnya pasangan elektron di orbital px, timah diubah menjadi ion Sn2+ dan konfigurasi elektronik yang dihasilkan adalah 5s25 px0haldan0halz0, dengan semua orbital p yang tersedia untuk menerima tautan dari spesies lain.
Ion Cl- berkoordinasi dengan ion Sn2+ untuk menimbulkan timah klorida. Konfigurasi elektronik timah dalam garam ini adalah 5s25 px2haldan2halz0, mampu menerima pasangan elektron lain dalam p orbital bebasnyaz.
Misalnya, Anda dapat menerima ion Cl lainnya-, membentuk kompleks geometri bidang trigonal (piramida dengan dasar segitiga) dan bermuatan negatif [SnCl3]-.
Reaktivitas
SnCl2 memiliki reaktivitas tinggi dan kecenderungan berperilaku seperti asam Lewis (reseptor elektron) untuk menyelesaikan oktet valensi.
Sama seperti ia menerima ion Cl-, hal yang sama terjadi dengan air, yang "menghidrasi" atom timah dengan menghubungkan molekul air secara langsung dengan timah, dan molekul air kedua membentuk interaksi ikatan hidrogen dengan yang pertama..
Hasil dari ini adalah bahwa SnCl2 tidak murni, tetapi terkoordinasi dengan air dalam garam dihidrasi: SnCl2· 2 jam2O.
SnCl2 Ini sangat larut dalam air dan pelarut polar, karena merupakan senyawa polar. Namun, kelarutannya dalam air, kurang dari berat massanya, mengaktifkan reaksi hidrolisis (pecahnya molekul air) untuk menghasilkan garam basa dan tidak larut:
SnCl2(aq) + H2O (l) <=> Sn (OH) Cl (s) + HCl (aq)
Panah ganda menunjukkan bahwa keseimbangan terbentuk, disukai ke kiri (menuju reaktan) jika konsentrasi HCl meningkat. Untuk ini, solusi SnCl2 digunakan memiliki pH asam, untuk menghindari pengendapan produk garam hidrolisis yang tidak diinginkan.
Aktivitas reduktif
Bereaksi dengan oksigen di udara untuk membentuk timah (IV) klorida atau stannik klorida:
6 SnCl2(aq) + O2(g) + 2H2O (l) => 2SnCl4(aq) + 4Sn (OH) Cl (s)
Dalam reaksi ini, timah teroksidasi membentuk ikatan dengan atom oksigen elektronegatif dan meningkatkan jumlah ikatannya dengan atom klor.
Secara umum, atom elektronegatif dari halogen (F, Cl, Br dan I) menstabilkan ikatan senyawa Sn (IV) dan fakta ini menjelaskan mengapa SnCl2 itu adalah agen pereduksi.
Ketika mengoksidasi dan kehilangan semua elektron valensi, ion Sn4+ tetap dengan konfigurasi 5s05 px0haldan0halz0, menjadi pasangan elektron dalam orbital 5s yang paling sulit untuk "disambar".
Struktur kimia
SnCl2 menyajikan struktur kristal tipe ortorombik, mirip dengan barisan gergaji, di mana ujung gigi adalah klorida.
Setiap baris adalah rantai SnCl3 membentuk jembatan Cl dengan atom Sn lainnya (Cl-Sn (Cl)2-Cl- ···), seperti dapat dilihat pada gambar di atas. Dua rantai, dihubungkan oleh interaksi lemah dari tipe Sn-Cl, merupakan satu lapisan susunan, yang ditumpangkan pada lapisan lain, dan seterusnya sampai padatan kristalin ditentukan..
Pasangan elektron bebas 5s2 menyebabkan distorsi dalam struktur karena menempati volume (volume awan elektronik).
Sn dapat memiliki bilangan koordinasi sama dengan sembilan, yang sama dengan memiliki sembilan tetangga, menggambar prisma trigonal dengan ini terletak di tengah-tengah gambar geometris dan Cl dalam simpul, di samping Cl lain yang terletak di masing-masing wajah persegi prisma.
Ini lebih mudah untuk diamati jika seseorang menganggap rantai di mana Sn (bola abu-abu gelap) menunjuk ke atas, dan tiga Cl yang terhubung dengannya membentuk lantai segitiga, sedangkan tiga Cl atas membentuk atap segitiga..
Penggunaan
Dalam sintesis organik digunakan sebagai pereduksi untuk senyawa nitro aromatik (Ar-NO2 à Ar-NH2). Karena struktur kimianya adalah laminar, ia digunakan di dunia katalisis reaksi organik, selain menjadi kandidat potensial untuk dukungan katalitik.
Sifat pereduksi digunakan untuk menentukan keberadaan senyawa emas, untuk melapisi kacamata dengan cermin perak dan untuk bertindak sebagai antioksidan.
Juga, dalam piramida trigonal geometri molekulnya (: SnX3- M.+) digunakan sebagai basa Lewis untuk sintesis sejumlah besar senyawa (seperti kompleks kluster Pt)3Sn8Cl20, di mana pasangan bebas elektron dikoordinasikan dengan asam Lewis).
Risiko
SnCl2 Ini dapat merusak sel darah putih. Ini korosif, iritan, karsinogenik, dan memiliki dampak negatif yang tinggi pada spesies yang mendiami ekosistem laut.
Ini dapat terurai pada suhu tinggi, melepaskan gas klor yang berbahaya. Dalam kontak dengan zat pengoksidasi tinggi, itu memicu reaksi eksplosif.
Referensi
- Menggigil & Atkins. (2008). Kimia anorganik Masuk Unsur-unsur kelompok 14 (edisi keempat., halaman 329). Mc Graw Hill.
- Buku Kimia. (2017). Diperoleh pada 21 Maret 2018, dari ChemicalBook: chemicalbook.com
- PubChem. (2018). Timah klorida. Diperoleh pada 21 Maret 2018, dari PubChem: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2017). Timah (II) klorida. Diperoleh pada 21 Maret 2018, dari Wikipedia: en.wikipedia.org
- E. G. Rochow, E. W. (1975). Kimia Germanium: Timah dan Timbal (ed pertama.). p-82.83. Pergamom Tekan.
- F. Hulliger. (1976). Kimia Struktural Fase-Tipe Lapisan. P-120.121. D. Perusahaan Penerbit Reidel.



