Formula Sodium Acetate, Persiapan, Properti, Risiko dan Penggunaan
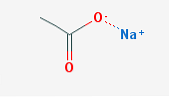
itu natrium asetat, juga dikenal sebagai natrium etanoat (disingkat NaOAc), adalah garam natrium asam asetat. Formula kimianya adalah CH3COONa dan memiliki ikatan ion antara ion natrium dan ion asetat.
Senyawa kimia ini secara alami hadir dalam jaringan tanaman dan hewan. Dapat ditemukan dalam bentuk apa pun, anhidrat atau trihidrat. Kedua ion, Na + dan CH3COO- hadir dalam organisme dan melakukan fungsi-fungsi vital: ion natrium sebagai pengatur total air tubuh dan ion asetat sebagai akseptor hidrogen (Formula Sodium asetat, 2005-2017).
Indeks
- 1 Persiapan
- 2 Sifat fisik dan kimia
- 3 Reaktivitas dan bahaya
- 4 Penanganan dan penyimpanan
- 5 Penggunaan dan aplikasi
- 6 Referensi
Persiapan
Sodium asetat adalah senyawa yang dapat disiapkan secara sederhana dan mudah diakses oleh siapa saja. Umumnya persiapannya dikenal sebagai "eksperimen es panas", karena kristalisasi menyerupai air dalam keadaan padat (ilmuwan, 2016).
Untuk menyiapkan natrium asetat, Anda hanya perlu cuka (asam asetat) dan natrium karbonat atau natrium bikarbonat. Cukup tambahkan bikarbonat ke dalam cuka, menghasilkan reaksi efervesen karena melepaskan karbon dioksida sesuai dengan reaksi.
CH3COOH + NaHCO3 → CH3COONa + H2CO3
H2CO3 → CO2 + H2O
Karbonat atau natrium bikarbonat dapat disubstitusi oleh natrium hidroksida (alkali) di mana natrium asetat dan air diproduksi sesuai dengan reaksi:
CH3COOH + NaOH → CH3COONa + H2O
Reaksi ini tidak menyebabkan efervesensi, tetapi memiliki kelemahan yaitu natrium hidroksida lebih sulit ditangani daripada bikarbonat..
Untuk mendapatkan efek kristalisasi (atau efek es panas) larutan harus jenuh dengan memanaskannya agar terlarut secara bikarbonat. Wadah yang tertutup kemudian didinginkan dan kemudian dipasang kembali. Selanjutnya, kristal disaring dan dihancurkan untuk penyimpanan (degroof, S.F.).
Sifat fisik dan kimia
Sodium asetat adalah gelas higroskopis putih dengan bau cuka.

Dalam hal bentuk senyawa anhidrat, senyawa ini memiliki berat molekul 82,03 g / mol dan kerapatan 1,5 g / ml. Titik leburnya adalah 324 derajat Celcius dan titik didihnya 881,4 derajat Celcius.
Dalam bentuk trihidratnya, ia memiliki berat molekul 136,03 g / mol dan kepadatan 1,45 g / ml. Titik lebur dan titik didih masing-masing turun secara drastis menjadi 58 derajat Celcius dan 122 derajat Celcius.
Sodium asetat sangat larut dalam air. Kelarutan bentuk trihidrat adalah 46,5 g natrium asetat dalam 100 ml air pada 20 derajat celcius, dan dalam bentuk anhidratnya dapat melarutkan 123 gram per 100 ml air (National Center for Biotechnology Information, 2017 ).
Kedua bentuk larut dalam aseton, metanol, hidrazin dan bentuk trihidrat larut dalam etanol. Sodium asetat memiliki struktur kristal monoklinik (Royal Society of Chemistry, 2015).
Sodium asetat adalah basa konjugat dari asam asetat, sehingga Anda dapat menggunakan larutan asam asetat / natrium asetat untuk menyiapkan larutan buffer, untuk mengontrol pH.
Larutan natrium asetat dalam air bersifat basa lemah. Ketika panas lebih tinggi dari 324 derajat Celcius, garam ini terurai, menghasilkan asap asam asetat.
Reaktivitas dan bahaya
Sodium asetat diklasifikasikan sebagai senyawa stabil dan tidak sesuai dengan zat pengoksidasi. Ketika dipanaskan dapat menghasilkan uap asam asetat dan melepaskan CO2. Senyawa ini dapat terbakar pada suhu tinggi melepaskan CO dan CO2.
Keamanan natrium asetat telah dipelajari secara luas dalam model binatang tikus dan tikus. Ketika diberikan secara oral, dosis mematikan yang membunuh setengah dari populasi tikus adalah 3530 mg natrium asetat per kg berat badan tikus..
Jika dihirup alih-alih dicerna, dosis yang diperlukan untuk membunuh setengah dari populasi tikus jauh lebih tinggi, lebih dari 30 g / m3 per jam.
Pada tikus, injeksi subkutan atau subkutan dengan berat 3200 mg / kg akan membunuh setengah populasi tikus, mirip dengan konsumsi natrium asetat pada tikus..
Namun pada tikus ketika diberikan secara oral, mereka dapat bertahan lebih dari tikus; menjadi dosis mematikan untuk setengah populasi tikus 6891 mg / kg berat badan.
Pada manusia, menghirup natrium asetat dapat menyebabkan batuk dan sakit tenggorokan, sementara kontak langsung dengan kulit atau mata dapat menyebabkan kemerahan dan iritasi. Namun, dan secara umum, toksisitas pada manusia minimal (WASSERMAN, 2015).
Ini dapat menyebabkan iritasi pada saluran pencernaan dengan sakit perut, mual, muntah dan mempengaruhi sistem kemih. Menghirup senyawa dapat menyebabkan iritasi pada saluran pernapasan. Gejala mungkin termasuk batuk, sakit tenggorokan, sesak napas dan nyeri dada.
Dalam kasus kontak dengan mata, lensa kontak harus diperiksa dan dihilangkan. Mata harus segera dicuci dengan banyak air selama minimal 15 menit. Anda bisa menggunakan air dingin. Perhatian medis harus diperoleh jika terjadi iritasi.
Jika terkena kulit, harus dicuci dengan sabun dan air. Anda bisa menggunakan air dingin. Kulit yang teriritasi ditutupi dengan emolien. Seperti halnya kontak mata, perhatian medis harus diperoleh jika iritasi berkembang.
Jika terhirup, korban harus dipindahkan ke tempat yang dingin. Jika tidak bernafas, pernapasan buatan harus diberikan. Jika sulit bernafas, oksigen harus disediakan. Sekali lagi, perlu segera mendapatkan perhatian medis.
Jika tertelan, muntah tidak boleh diinduksi kecuali diindikasikan secara tertulis oleh petugas medis. Jangan pernah memberikan apapun melalui mulut kepada orang yang tidak sadar.
Pakaian longgar seperti kerah kemeja, dasi atau ikat pinggang harus dilonggarkan. Perhatian medis harus diperoleh jika gejala muncul (Material Safety Data Sheet Sodium acetate anhydrous, 2013).
Penanganan dan penyimpanan
-Senyawa harus dijauhkan dari panas dan sumber nyala
-Wadah kosong menimbulkan bahaya kebakaran, menguapkan residu di bawah tudung ekstraktor
-Peralatan listrik harus dibumikan untuk menghindari percikan
-Jangan menelan atau menghirup debu
-Pakaian pelindung yang tepat harus dikenakan
-Dalam hal kurangnya ventilasi, peralatan pernapasan yang memadai harus dipakai
-Jika tertelan, Anda harus segera pergi ke dokter dan menunjukkan wadah atau label
-Pereaksi harus dijauhkan dari bahan-bahan yang tidak cocok seperti zat pengoksidasi dan asam.
-Simpan wadah tertutup rapat, selain menjaga wadah tetap dingin dan berventilasi baik.
Penggunaan dan aplikasi
Sodium asetat digunakan dalam berbagai industri yang sangat beragam. Dalam industri tekstil, natrium asetat menetralkan aliran limbah asam sulfat dan juga sebagai fotoresis, sambil menggunakan pewarna anilin. Ini meningkatkan kualitas kain jadi.
Dalam foto itu, natrium asetat adalah bagian dari solusi pengembang dan bertindak sebagai fotoresis. Sodium asetat digunakan untuk mengurangi kerusakan yang disebabkan oleh air ke beton dengan bertindak sebagai sealant, sementara ramah lingkungan dan lebih murah daripada alternatif epoksi yang biasa digunakan untuk menutup beton terhadap penetrasi air..
Ini juga merupakan agen pengawet dalam penyamakan kromium dan membantu mencegah vulkanisasi kloroprena dalam produksi karet sintetis. Dalam pengolahan kapas untuk bantalan kapas sekali pakai, natrium asetat digunakan untuk menghilangkan penumpukan listrik statis.
Sodium asetat yang ditambahkan ke dalam makanan berperan sebagai pengawet, dan zat penyedap. Secara khusus, keripik kentang dengan natrium asetat memiliki rasa "garam dan cuka" yang khas.
Sodium asetat juga digunakan dalam bantalan pemanas, penghangat tangan dan es panas. Kristal natrium asetat trihidrat dilelehkan pada suhu 58,4 ° C, larut dalam air kristalisasi.
Ketika dipanaskan di luar titik leleh dan kemudian dibiarkan dingin, larutan encer menjadi jenuh. Solusi ini mampu mendingin hingga suhu kamar tanpa membentuk kristal.
Dengan menekan cakram logam ke bantalan pemanas, pusat nukleasi terbentuk, menyebabkan solusi mengkristal kembali menjadi natrium asetat padat trihidrat. Proses pembentukan ikatan kristalisasi adalah eksoterm. Panas fusi laten adalah sekitar 264-289 kJ / kg.
Tidak seperti beberapa jenis paket panas, seperti yang bergantung pada reaksi kimia yang ireversibel, paket panas natrium asetat dapat dengan mudah digunakan kembali dengan merendam paket dalam air mendidih selama beberapa menit, sampai kristal larut sepenuhnya dan memungkinkan bahwa pak mendingin perlahan hingga mencapai suhu kamar.
Solusi natrium asetat dan asam asetat bertindak sebagai buffer untuk mempertahankan pH yang relatif konstan, sifat yang berguna untuk reaksi riset biokimia maupun untuk industri minyak dan industri kosmetik.
Sodium asetat dapat digunakan untuk pengendapan asam nukleat kecil. Curah hujan ini dapat digunakan untuk mengkonsentrasikan asam nukleat kecil dari larutan encer seperti buffer berfungsi lebih rendah setelah fraksinasi flashPAGE.
Ketika kurang dari 2 μg asam nukleat dimasukkan ke dalam shredder flashPAGE, curah hujan dengan natrium asetat / etanol direkomendasikan semalam dengan kendaraan seperti linear akrilamida atau glikogen, untuk pemulihan maksimum asam nukleat dari buffer berjalan lambat.
Penggunaan glikogen sebagai pembawa tidak dianjurkan untuk sampel yang akan digunakan untuk analisis chip DNA (Sodium Acetate Presipitasi of Small Nucleic Acids, S.F.).
Di bidang kedokteran, larutan natrium asetat mengobati pasien dengan kadar asam darah tinggi dan / atau kadar natrium rendah.
Sodium adalah kation utama cairan ekstraseluler. Ini terdiri lebih dari 90% dari total kation pada konsentrasi plasma normal sekitar 140 mEq / liter. Ion natrium memainkan peran penting dalam kontrol total air tubuh dan distribusinya (Sodium Acetate, 2010).
Asetat adalah akseptor ion hidrogen. Ini juga berfungsi sebagai sumber alternatif bikarbonat (HCO3-) untuk konversi metabolisme di hati. Konversi ini telah terbukti berjalan dengan mudah, bahkan di hadapan penyakit hati yang parah.
Suntikan natrium asetat yang dilarutkan dalam air diberikan secara intravena sebagai pengganti elektrolit. Setiap 20 ml mengandung 3,28 g natrium asetat yang menghasilkan 40 mEq natrium (Na +) dan asetat (HCO)3-). Solusinya tidak mengandung bakteriostat, agen antimikroba atau buffer tambahan. Ini mungkin mengandung asam asetat untuk penyesuaian pH (pH 6.5 (6.0 ke 7.0)). Konsentrasi osmolar adalah 4 mOsmol / ml (kalk).
Solusinya dianggap sebagai alternatif untuk natrium klorida untuk memberikan ion natrium (Na +) untuk penambahan cairan infus volume tinggi untuk penggunaan intravena (Sodium Acetate, 2009).
Solusi yang mengandung ion natrium harus digunakan dengan sangat hati-hati, terutama dalam kasus pasien dengan gagal jantung kongestif, gagal ginjal berat dan dalam kondisi klinis di mana terdapat edema dengan retensi natrium.
Pada pasien dengan gangguan fungsi ginjal, pemberian larutan yang mengandung ion natrium dapat menyebabkan retensi natrium. Solusi yang mengandung ion asetat harus digunakan dengan sangat hati-hati pada pasien dengan alkalosis metabolik atau pernapasan.
Asetat harus diberikan dengan sangat hati-hati dalam kondisi di mana ada peningkatan kadar atau gangguan penggunaan ion ini, seperti insufisiensi hati yang parah..
Referensi
- (S.F.). Cara Membuat Natrium Asetat Dari Bahan-Bahan Rumah Tangga. Recuperado de instructables: instructables.com.
- Lembar Data Keselamatan Bahan Sodium asetat anhidrat. (2013, 21 Mei). Diperoleh dari sciencelab: sciencelab.com.
- Pusat Nasional untuk Informasi Bioteknologi. (2017, 4 Maret). Basis Data Gabungan PubChem; CID = 517045. Diperoleh dari PubChem.
- Royal Society of Chemistry. (2015). Sodium asetat. Diperoleh dari chemspider.com.
- ilmuwan, D. N.-c. (2016, 12 Agustus). "HOT ICE" - eksperimen luar biasa. Diperoleh dari youtube.com.
- Sodium Acetate. (2009, 19 Mei). Diperoleh dari rxlist.
- Sodium Acetate. (2010, April). Sembuh dari drugs.com.
- Formula natrium asetat. (2005-2017). Dipulihkan dari softschools.com.
- Pengendapan Sodium Asetat Asam Nukleat Kecil. (S.F.). Dipulihkan dari thermofisher.
- WASSERMAN, R. (2015, 16 Agustus). Apa itu Sodium Acetate Salt? Diperoleh dari livestrong: livestrong.com.


