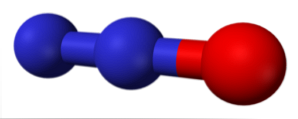
Nitrogen Oksida (NOx) Formulasi dan Nomenklatur yang Berbeda
itu nitrogen oksida mereka pada dasarnya adalah senyawa anorganik gas yang mengandung ikatan antara atom nitrogen dan oksigen. Formula kimia kelompoknya adalah TIDAKx, menunjukkan bahwa oksida memiliki proporsi oksigen dan nitrogen yang berbeda.
Nitrogen memimpin kelompok 15 dari tabel periodik, sedangkan kelompok oksigen 16; kedua elemen adalah anggota periode 2. Kedekatan ini adalah alasan mengapa ikatan N-O kovalen dalam oksida. Dengan cara ini, ikatan dalam nitrogen oksida bersifat kovalen.
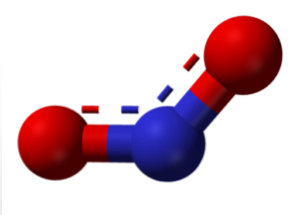
Semua hubungan ini dapat dijelaskan dengan menggunakan teori orbital molekul, yang mengungkap paramagnetisme (sebuah elektron yang tidak berpasangan pada orbital molekul terakhir) dari beberapa senyawa ini. Dari jumlah tersebut, senyawa yang paling umum adalah nitrat oksida dan nitrogen dioksida.
Molekul dalam gambar atas sesuai dengan struktur sudut dalam fase gas nitrogen dioksida (NO2). Sebaliknya, nitric oxide (NO) memiliki struktur linier (mempertimbangkan hibridisasi sp untuk kedua atom).
Nitrogen oksida adalah gas yang diproduksi oleh banyak aktivitas manusia, dari mengendarai kendaraan atau merokok, hingga proses industri sebagai limbah pencemar. Namun, NO secara alami dihasilkan oleh reaksi enzimatik dan kilat dalam badai petir: N2(g) + O2(g) => 2NO (g)
Suhu tinggi dari sinar memecah penghalang energetik yang mencegah reaksi ini terjadi dalam kondisi normal. Penghalang energi apa? Itu dibentuk oleh ikatan rangkap N≡N, membuat molekul-N2 gas inert dari atmosfer.
Indeks
- 1 Bilangan oksidasi untuk nitrogen dan oksigen dalam oksida mereka
- 2 formulasi dan nomenklatur yang berbeda
- 2.1 Nitrous oxide (N2O)
- 2.2 Nitric oxide (NO)
- 2.3 Nitrogen trioksida (N2O3)
- 2.4 Dioksida dan nitrogen tetroksida (NO2, N2O4)
- 2.5 Dinitrogen pentoxide (N2O5)
- 3 Referensi
Bilangan oksidasi untuk nitrogen dan oksigen dalam oksida mereka
Konfigurasi elektronik untuk oksigen adalah [He] 2s22p4, hanya membutuhkan dua elektron untuk menyelesaikan oktet dari cangkang valensinya; yaitu, ia dapat memperoleh dua elektron dan memiliki bilangan oksidasi sama dengan -2.
Di sisi lain, konfigurasi elektronik untuk nitrogen adalah [He] 2s22p3, mampu memperoleh hingga tiga elektron untuk mengisi oktet valensi; misalnya, dalam kasus amonia (NH3) memiliki bilangan oksidasi sama dengan -3. Tetapi oksigen jauh lebih elektronegatif daripada hidrogen dan "memaksa" nitrogen untuk berbagi elektronnya.
Berapa banyak elektron yang dapat dibagi nitrogen dengan oksigen? Jika Anda berbagi elektron dari kulit valensi Anda satu per satu, Anda akan mencapai batas lima elektron, sesuai dengan jumlah oksidasi +5.
Akibatnya, tergantung pada berapa banyak ikatan yang terbentuk dengan oksigen, bilangan oksidasi nitrogen bervariasi dari +1 hingga +5.
Formulasi dan nomenklatur berbeda
Nitrogen oksida, dalam urutan peningkatan jumlah oksidasi nitrogen, adalah:
- N2Atau, dinitrogen oksida (+1)
- NO, nitric oxide (+2)
- N2O3, dinitrogen trioxide (+3)
- TIDAK2, nitrogen dioxide (+4)
- N2O5, dinitrogen pentoxide (+5)
Nitrous oxide (N2O)
Nitrous oxide (atau yang dikenal sebagai gas tertawa) adalah gas yang tidak berwarna, dengan sedikit aroma manis dan sedikit reaktif. Ini dapat divisualisasikan sebagai molekul N2 (bola biru) yang telah menambahkan atom oksigen di satu ujung. Ini disiapkan oleh dekomposisi termal garam nitrat dan digunakan sebagai anestesi dan analgesik.
Nitrogen memiliki bilangan oksidasi +1 dalam oksida ini, yang berarti ia tidak terlalu teroksidasi dan permintaannya terhadap elektron tidak menarik; namun, Anda hanya perlu mendapatkan dua elektron (satu untuk setiap nitrogen) untuk menjadi nitrogen molekul yang stabil.
Dalam larutan basa dan asam, reaksinya adalah:
N2O (g) + 2H+(ac) + 2e- => N2(g) + H2O (l)
N2O (g) + H2O (l) + 2e- => N2(g) + 2OH-(ac)
Reaksi-reaksi ini, walaupun secara termodinamik lebih disukai oleh pembentukan molekul N yang stabil2, terjadi perlahan dan reagen yang menyumbangkan pasangan elektron harus sangat kuat mereduksi agen.
Nitric oxide (NO)
Oksida ini terdiri dari gas tidak berwarna, reaktif dan paramagnetik. Seperti nitro oksida, ia memiliki struktur molekul linier, tetapi dengan perbedaan besar bahwa ikatan N = O juga memiliki karakter ikatan rangkap tiga..
NO teroksidasi dengan cepat di udara untuk menghasilkan NO2, dan karenanya menghasilkan orbital molekul yang lebih stabil dengan atom nitrogen yang lebih teroksidasi (+4).
2NO (g) + O2(g) => 2NO2(g)
Studi biokimia dan fisiologis berada di belakang peran jinak oksida ini dalam organisme hidup.
Ia tidak dapat membentuk ikatan N-N dengan molekul NO lainnya karena delokalisasi elektron tidak berpasangan dalam orbital molekul, yang lebih mengarah ke atom oksigen (karena elektronegativitasnya yang tinggi). Kebalikannya terjadi dengan NO2, yang dapat membentuk dimer gas.
Nitrogen trioksida (N2O3)
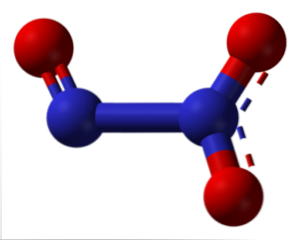
Garis putus-putus dari struktur menunjukkan resonansi ikatan rangkap. Seperti semua atom, mereka memiliki hibridisasi sp2, molekulnya rata dan interaksi molekuler cukup efektif agar nitrogen trioksida ada sebagai padatan biru di bawah -101ºC. Pada suhu yang lebih tinggi meleleh dan terdisosiasi menjadi NO dan NO2.
Mengapa itu dipisahkan? Karena bilangan oksidasi +2 dan +4 lebih stabil daripada +3, bilangan oksidasi hadir dalam oksida untuk masing-masing dari dua atom nitrogen. Ini, sekali lagi, dapat dijelaskan oleh stabilitas orbital molekul yang dihasilkan dari disproporsi.
Pada gambar, sisi kiri N2O3 berkorespondensi dengan NO, sedangkan sisi kanan NO2. Logikanya, diproduksi oleh koalesensi oksida sebelumnya pada suhu yang sangat dingin (-20ºC). N2O3 adalah asam nitrat anhidrida (HNO2).
Dioksida dan nitrogen tetroksida (NO2, N2O4)
TIDAK2 itu adalah gas coklat atau coklat, reaktif dan paramagnetik. Karena memiliki elektron yang tidak berpasangan, ia meredup (mengikat) dengan molekul gas NO lainnya2 untuk membentuk nitrogen tetroksida, gas tidak berwarna, membangun keseimbangan antara kedua spesies kimia:
2NO2(g) <=> N2O4(g)
Ini adalah zat pengoksidasi beracun dan serbaguna, mampu tidak proporsional dalam reaksi redoks dalam ion (oksoanion).2- dan TIDAK3- (menghasilkan hujan asam), atau dalam NO.
Demikian juga, TIDAK2 terlibat dalam reaksi atmosfer kompleks yang menyebabkan variasi konsentrasi ozon (OR3) di tingkat terestrial dan di stratosfer.
Dinitrogen pentoxide (N2O5)
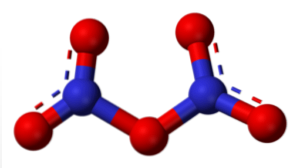
Ketika terhidrasi, itu menghasilkan HNO3, dan pada konsentrasi asam yang lebih tinggi, oksigen terutama terprotonasi dengan muatan positif parsial -O+-H, mempercepat reaksi redoks
Referensi
- askIITians. ((2006-2018)). askIITians. Diperoleh pada 29 Maret 2018, dari askIITians: askiitians.com
- Encyclopaedia Britannica, Inc. (2018). Encyclopaedia Britannica. Diperoleh pada 29 Maret 2018, dari Encyclopaedia Britannica: britannica.com
- Kota Racun. (2017). Kota Racun. Diperoleh pada 29 Maret 2018, dari Tox Town: toxtown.nlm.nih.gov
- Profesor Patricia Shapley. (2010). Nitrogen Oksida di Atmosfer. Universitas Illinois. Diperoleh pada 29 Maret 2018, dari: butane.chem.uiuc.edu
- Menggigil & Atkins. (2008). Kimia anorganik Masuk Unsur-unsur kelompok 15. (Edisi keempat., Hlm. 361-366). Mc Graw Hill