Emas oksida (III) (Au2O3) struktur, sifat, nomenklatur dan kegunaan
itu emas oksida (III) adalah senyawa anorganik yang rumus kimianya adalah Au2O3. Secara teoritis orang mungkin berharap sifatnya dari tipe kovalen. Namun, keberadaan karakter ionik tertentu dalam padatannya tidak dapat dibuang sama sekali; atau apa yang sama, asumsikan tidak adanya kuasi3+ di sebelah anion O2-.
Mungkin tampak kontradiktif bahwa emas, sebagai logam mulia, dapat berkarat. Dalam kondisi normal, keping emas (seperti bintang-bintang pada gambar di bawah) tidak dapat dioksidasi oleh kontak dengan oksigen di atmosfer; Namun, ketika diiradiasi dengan radiasi ultraviolet di hadapan ozon, OR3, gambarnya berbeda.

Jika bintang-bintang emas mengalami kondisi ini, mereka akan berubah menjadi coklat kemerahan, karakteristik Au2O3.
Metode lain untuk memperoleh oksida ini akan melibatkan perlakuan kimia dari bintang-bintang tersebut; misalnya, mengubah massa emas menjadi klorida masing-masing, AuCl3.
Setelah itu, ke AuCl3, dan sisa garam emas yang mungkin terbentuk, media dasar yang kuat ditambahkan; dan dengan ini, Anda mendapatkan oksida terhidrasi atau hidroksida, Au (OH)3. Akhirnya, senyawa terakhir ini mengalami dehidrasi termal untuk mendapatkan Au2O3.
Indeks
- 1 Struktur oksida emas (III)
- 1.1 Aspek elektronik
- 1.2 Menghidrasi
- 2 Properti
- 2.1 Penampilan fisik
- 2.2 Massa molekul
- 2.3 Kepadatan
- 2.4 Titik lebur
- 2.5 Stabilitas
- 2.6 Kelarutan
- 3 Nomenklatur
- 4 Penggunaan
- 4.1 Pewarnaan kacamata
- 4.2 Sintesis aurat dan emas fulminasi
- 4.3 Penanganan monolayer yang dirakit sendiri
- 5 Referensi
Struktur oksida emas (III)
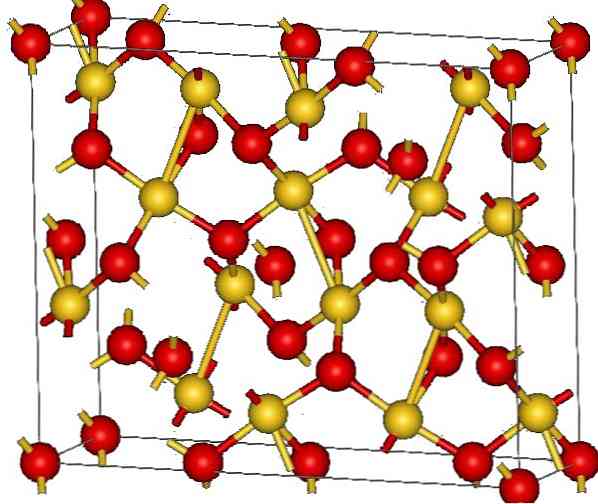
Struktur kristal emas (III) oksida ditunjukkan pada gambar atas. Susunan atom emas dan oksigen dalam padatan ditunjukkan, baik sebagai atom netral (padatan kovalen), atau sebagai ion (padatan ionik). Tidak jelas, cukup untuk menghilangkan atau menempatkan tautan Au-O dalam hal apa pun.
Menurut gambar, diasumsikan bahwa karakter kovalen mendominasi (yang logis). Untuk alasan itu, atom dan ikatan yang diwakili masing-masing ditunjukkan dengan bola dan bar. Bola emas sesuai dengan atom emas (AuIII-O), dan kemerahan pada atom oksigen.
Jika Anda perhatikan dengan teliti, Anda akan melihat bahwa ada unit AuO4, yang bergabung dengan atom oksigen. Cara lain untuk memvisualisasikannya adalah dengan mempertimbangkan setiap Au3+ dikelilingi oleh empat O2-; Tentu saja, dari perspektif ionik.
Struktur ini kristalin karena atom diperintahkan mematuhi pola jarak jauh yang sama. Jadi, sel kesatuannya berhubungan dengan sistem kristal rombohedral (sama seperti pada gambar atas). Karena itu, semua Au2O3 bisa dibangun jika semua bidang sel unit didistribusikan di ruang angkasa.
Aspek elektronik
Emas adalah logam transisi, dan diharapkan bahwa orbital 5d-nya berinteraksi langsung dengan orbital 2p dari atom oksigen. Tumpang tindih orbital mereka secara teoritis akan menghasilkan pita konduksi, yang akan mengkonversi Au2O3 dalam semikonduktor yang solid.
Oleh karena itu, struktur Au yang sebenarnya2O3 bahkan lebih kompleks dengan pemikiran ini.
Menghidrasi
Emas oksida dapat mempertahankan molekul air dalam kristal rhombohedralnya, yang menimbulkan hidrat. Ketika hidrat tersebut terbentuk, struktur menjadi amorf, yaitu tidak teratur.
Formula kimia untuk hidrat semacam itu dapat berupa salah satu dari yang berikut, yang sebenarnya tidak diklarifikasi secara mendalam: Au2O3∙ zH2O (z = 1, 2, 3, dll.), Au (OH)3, atau AuxOdan(OH)z.
Formula Au (OH)3 mewakili penyederhanaan yang berlebihan dari komposisi sebenarnya dari hidrat tersebut. Ini karena dalam hidroksida emas (III), para peneliti juga telah menemukan keberadaan Au2O3; dan karenanya, masuk akal untuk memperlakukannya secara terpisah sebagai logam transisi hidroksida "sederhana".
Di sisi lain, dari padatan dengan formula AuxOdan(OH)z struktur amorf bisa diharapkan; karena, ini tergantung pada koefisien x, dan dan z, yang variasinya akan memunculkan semua jenis struktur yang sulit menunjukkan pola kristal.
Properti
Penampilan fisik
Ini adalah padatan coklat kemerahan.
Massa molekul
441,93 g / mol.
Kepadatan
11,34 g / mL.
Titik lebur
Ini meleleh dan terurai pada 160ºC. Karena itu tidak memiliki titik didih, sehingga oksida ini tidak pernah mencapai titik didih.
Stabilitas
Au2O3 itu secara termodinamik tidak stabil karena, seperti yang disebutkan di awal, emas cenderung tidak teroksidasi dalam kondisi suhu normal. Jadi mudah direduksi menjadi emas mulia lagi.
Semakin tinggi suhunya, semakin cepat reaksinya, yang dikenal sebagai dekomposisi termal. Jadi, Au2O3 pada 160 ° C terurai untuk menghasilkan emas logam dan melepaskan oksigen molekul:
2 Au2O3 => 4 Au + 3 O2
Reaksi yang sangat mirip dapat terjadi dengan senyawa lain yang mendukung reduksi tersebut. Mengapa reduksi? Karena emas kembali untuk mendapatkan elektron yang diambil oksigen darinya; yang sama dengan mengatakan bahwa ia kehilangan hubungan dengan oksigen.
Kelarutan
Ini adalah padatan yang tidak larut dalam air. Namun, larut dalam asam klorida dan asam nitrat, karena pembentukan emas klorida dan nitrat.
Nomenklatur
Emas oksida (III) adalah nama yang diatur oleh nomenklatur saham. Cara lain untuk menyebutkannya adalah:
-Nomenklatur tradisional: aureric oxide, karena valensi 3+ adalah yang tertinggi untuk emas.
-Nomenklatur sistematis: dioro trioxide.
Penggunaan
Pewarnaan kacamata
Salah satu kegunaannya yang paling terkenal adalah memberikan warna kemerahan pada bahan tertentu, seperti kacamata, selain memberikan sifat tertentu yang melekat pada atom emas..
Sintesis aurat dan emas fulminasi
Jika Au ditambahkan2O3 ke media di mana ia larut, dan di hadapan logam, aurat dapat mengendap setelah penambahan basa kuat; yang, dibentuk oleh anion AuO4- di perusahaan kation logam.
Juga, Au2O3 bereaksi dengan amonia untuk membentuk senyawa fulminasi emas, Au2O3(NH3)4. Namanya berasal dari fakta bahwa itu sangat eksplosif.
Penanganan monolayer rakitan
Pada emas dan oksidanya, senyawa tertentu, seperti dialkil disulfida, RSSR, tidak diserap dengan cara yang sama. Ketika adsorpsi ini terjadi, ikatan Au-S terbentuk secara spontan, di mana atom belerang menunjukkan dan mendefinisikan karakteristik kimiawi permukaan tersebut tergantung pada gugus fungsi yang terikat..
RSSR tidak dapat menyerap pada Au2O3, tetapi pada emas metalik. Oleh karena itu, jika permukaan emas dan tingkat oksidasi dimodifikasi, serta ukuran partikel atau lapisan Au2O3, permukaan yang lebih heterogen dapat dirancang.
Au permukaan ini2O3-AuSR berinteraksi dengan oksida logam perangkat elektronik tertentu, sehingga mengembangkan permukaan yang lebih cerdas di masa depan.
Referensi
- Wikipedia. (2018). Emas (III) oksida. Diperoleh dari: en.wikipedia.org
- Formulasi kimia (2018). Emas oksida (III). Dipulihkan dari: formulacionquimica.com
- D. Michaud. (24 Oktober 2016). Oksida emas. 911 Ahli Metalurgi. Diperoleh dari: 911metallurgist.com
- Shi, R. Asahi dan C. Stampfl. (2007). Properti dari oksida emas Au2O3 dan Au2O: Investigasi prinsip pertama. Masyarakat Fisik Amerika.
- Cook, Kevin M. (2013). Emas Oksida sebagai Lapisan Masking untuk Kimia Permukaan Regioselektif. Tesis dan Disertasi. Kertas 1460.


