Sifat-sifat etil eter, struktur, perolehan, penggunaan
itu etil eter, juga dikenal sebagai dietil eter, adalah senyawa organik yang rumus kimianya adalah C4H10O. Ini ditandai dengan menjadi cairan yang tidak berwarna dan mudah menguap, dan oleh karena itu, botol-botolnya harus tetap tertutup rapat mungkin..
Eter ini diklasifikasikan sebagai anggota eter dialkil; yaitu, mereka memiliki rumus ROR ', di mana R dan R' mewakili segmen karbon yang berbeda. Dan seperti yang menggambarkan nama tengahnya, dietil eter, adalah dua radikal-etil yang mengikat atom oksigen.

Awalnya etil eter digunakan sebagai anestesi umum, diperkenalkan pada tahun 1846 oleh William Thomas Green Morton. Namun, karena sifatnya yang mudah terbakar, penggunaannya ditolak, menggantikannya dengan anestesi yang kurang berbahaya lainnya..
Senyawa ini juga telah digunakan untuk memperkirakan waktu sirkulasi darah, selama penilaian status kardiovaskular pasien.
Di dalam tubuh, dietil eter dapat diubah menjadi karbon dioksida dan metabolit; yang terakhir akhirnya diekskresikan dalam urin. Namun, sebagian besar eter yang diberikan dihembuskan ke paru-paru, tanpa melalui modifikasi apa pun.
Di sisi lain, itu digunakan sebagai pelarut untuk sabun, minyak, parfum, alkaloid dan gusi.
Indeks
- 1 Struktur etil eter
- 1.1 Gaya antarmolekul
- 2 Sifat fisik dan kimia
- 2.1 Nama lain
- 2.2 Formula molekul
- 2.3 Berat molekul
- 2.4 Penampilan fisik
- 2.5 Bau
- 2.6 Rasa
- 2.7 Titik didih
- 2.8 Titik lebur
- 2.9 Titik nyala
- 2.10 Kelarutan dalam air
- 2.11 Kelarutan dalam cairan lain
- 2.12 Kepadatan
- 2.13 Kepadatan uap
- 2.14 Tekanan uap
- 2.15 Stabilitas
- 2.16 Pengapian otomatis
- 2.17 Penguraian
- 2.18 Viskositas
- 2.19 Panas terbakar
- 2.20 Panas penguapan
- 2.21 Ketegangan permukaan
- 2.22 Potensi ionisasi
- 2.23 Ambang bau
- 2.24 Indeks bias
- 3 Memperoleh
- 3.1 Dari etil alkohol
- 3.2 Dari etilena
- 4 Toksisitas
- 5 Penggunaan
- 5.1 Pelarut organik
- 5.2 Anestesi umum
- 5.3 Roh eter
- 5.4 Evaluasi sirkulasi darah
- 5.5 Laboratorium pengajaran
- 6 Referensi
Struktur etil eter
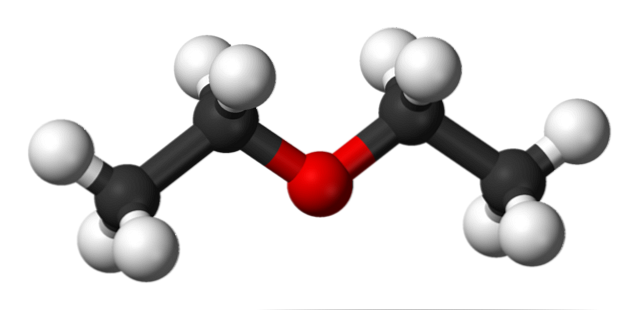
Pada gambar di atas kami memiliki representasi dengan model bola dan batang struktur molekul etil eter.
Seperti dapat dilihat, bola merah, yang sesuai dengan atom oksigen, memiliki dua gugus etil yang terhubung di kedua sisi. Semua tautan sederhana, fleksibel, dan dapat diputar secara bebas di sekitar sumbu σ.
Rotasi ini berasal stereoisomer yang dikenal sebagai konformer; bahwa lebih dari isomer, mereka adalah keadaan spasial alternatif. Struktur gambar sesuai persis dengan anti konformer, di mana semua kelompok atomnya terhuyung-huyung (terpisah satu sama lain).
Apa yang akan menjadi konformer lainnya? The gerhana, dan meskipun gambar Anda tidak tersedia, hanya memvisualisasikannya dengan bentuk U. Di ujung atas U akan ditemukan kelompok metil, -CH3, yang akan mengalami tolakan sterik (mereka akan bertabrakan di ruang angkasa).
Oleh karena itu, diharapkan molekul CH3CH2OCH2CH3 mengadopsi anti konformasi sebagian besar waktu.
Gaya antarmolekul
Dengan kekuatan intermolekul apa molekul etil eter diatur dalam fase cair? Mereka dipertahankan dalam cairan terutama berkat gaya dispersi, karena momen dipol mereka (1.5D) tidak memiliki daerah yang cukup kurang dalam kepadatan elektronik (δ +)
Ini karena tidak ada atom karbon dari gugus etil yang memberikan terlalu banyak kerapatan elektron pada atom oksigen. Di atas terbukti dengan peta potensi elektrostatik etil eter di tangan (gambar bawah). Perhatikan tidak adanya wilayah biru.
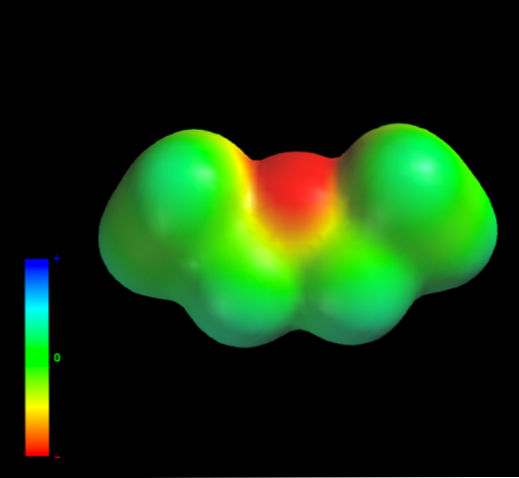
Oksigen juga tidak dapat membentuk ikatan hidrogen, karena tidak ada ikatan O-H yang tersedia dalam struktur molekul. Oleh karena itu, dipol instan dan massa molekulnya yang mendukung gaya dispersal mereka.
Meskipun demikian, sangat larut dalam air. Mengapa Karena atom oksigennya, dengan kerapatan elektron yang lebih tinggi, dapat menerima ikatan hidrogen dari molekul air:
(CH3CH2)2Oδ- - δ+H-OH
Interaksi ini bertanggung jawab atas 6.04g eter ini larut dalam 100 mL air.
Sifat fisik dan kimia
Nama lain
-Dietil eter
-Etoksietana
-Etil oksida
Rumus molekul
C4H10O atau (C2H5)2O.
Berat molekul
74,14 g / mol.
Penampilan fisik
Cairan tidak berwarna.
Bau
Manis dan pedas.
Rasa
Terbakar dan manis.
Titik didih
94,3 ºF (34,6 ºC) hingga 760 mmHg.
Titik lebur
-177,3 ºF (-116,3 ªC). Kristal yang stabil.
Titik penyalaan
-49ºF (wadah tertutup).
Kelarutan dalam air
6,04 g / 100 mL pada 25 ºC.
Kelarutan dalam cairan lain
Larut dengan alkohol alifatik rantai pendek, benzena, kloroform, petroleum eter, pelarut lemak, banyak minyak, dan asam klorida pekat.
Larut dalam aseton dan sangat larut dalam etanol. Ini juga larut dalam nafta, benzena dan minyak.
Kepadatan
0,714 mg / mL pada 68 ªF (20 ºC).
Kepadatan uap
2.55 (terkait dengan udara yang diambil dengan kepadatan 1).
Tekanan uap
442 mmHg pada 68ºF. 538 mmHg pada 25 ° C. 58,6 kPa pada 20 ºC.
Stabilitas
Ini perlahan teroksidasi oleh aksi udara, kelembaban dan cahaya dengan pembentukan peroksida.
Pembentukan peroksida dapat terjadi dalam wadah eter yang telah dibuka dan yang disimpan dalam penyimpanan selama lebih dari enam bulan. Peroksida dapat meledak melalui gesekan, benturan atau pemanasan.
Hindari kontak dengan: seng, halogen, oksihalida non-logam, zat pengoksidasi kuat, kromil klorida, minyak tementin, nitrat dan logam klorida.
Pengapian otomatis
356ºF (180ºC).
Dekomposisi
Saat memanaskannya terurai, mengeluarkan asap yang menyengat dan menjengkelkan.
Viskositas
0,2448 cPoise pada 20 ºC.
Panas terbakar
8.807 Kkal / g.
Panas penguapan
89,8 cal / g pada 30 ºC.
Ketegangan permukaan
17,06 dynes / cm pada 20º C.
Potensi ionisasi
9,53 eV.
Ambang bau
0,83 ppm (kemurnian tidak diberikan).
Indeks bias
1,355 pada 15 ºC.
Memperoleh
Dari etil alkohol
Etil eter dapat diperoleh dari etil alkohol, dengan adanya asam sulfat sebagai katalis. Asam sulfat dalam medium berair terdisosiasi menghasilkan ion hidronium, H3O+.
Etil alkohol anhidrat mengalir melalui larutan asam sulfat, dipanaskan antara 130 ° C dan 140 ° C, menghasilkan protonasi molekul etil alkohol. Selanjutnya, molekul lain dari etil alkohol non-protonasi bereaksi dengan molekul yang terprotonasi.
Ketika ini terjadi, serangan nukleofilik dari molekul kedua etil alkohol mendorong pelepasan air dari molekul pertama (yang terprotonasi); sebagai hasilnya, etil eter terprotonasi terbentuk (CH3CH2OHCH2CH3), dengan oksigen positif bermuatan sebagian.
Namun, metode sintesis ini kehilangan efisiensi karena asam sulfat diencerkan dengan air yang dihasilkan dalam proses (produk dehidrasi etil alkohol).
Suhu reaksi sangat penting. Pada suhu di bawah 130 ° C, reaksinya lambat dan sebagian besar etil alkohol akan didistilasi.
Di atas 150 ° C, asam sulfat menyebabkan pembentukan etilen (ikatan rangkap dua), alih-alih bergabung dengan etil alkohol untuk membentuk etil eter.
Dari etilena
Dalam proses yang berlawanan, yaitu hidrasi etilena dalam fase uap, etil eter dapat dibentuk sebagai produk sampingan selain etil alkohol. Bahkan, rute sintetis ini menghasilkan sebagian besar senyawa organik ini.
Proses ini menggunakan katalis asam fosfat yang difiksasi pada pendukung padat, yang dapat disesuaikan untuk menghasilkan lebih banyak eter.
Dehidrasi dalam fase uap etanol dengan adanya katalis alumina, dapat memberikan hasil 95% dalam produksi etil eter.
Toksisitas
Ini dapat menghasilkan iritasi pada kulit dan mata melalui kontak. Kontak dengan kulit dapat menyebabkan kulit menjadi kering dan pecah-pecah. Eter biasanya tidak menembus kulit, karena cepat menguap.
Iritasi mata yang disebabkan oleh eter biasanya ringan, dan dalam kasus iritasi parah, kerusakan biasanya dapat dibalikkan..
Konsumsinya menghasilkan efek narkotika dan iritasi lambung. Tertelan yang parah dapat menyebabkan kerusakan ginjal.
Menghirup eter dapat menyebabkan iritasi pada hidung dan tenggorokan. Dalam kasus inhalasi eter dapat terjadi: kantuk, kegembiraan, pusing, muntah, pernapasan tidak teratur dan peningkatan air liur.
Paparan yang tinggi dapat menyebabkan hilangnya kesadaran dan bahkan kematian.
OSHA menetapkan batas pajanan kerja rata-rata 800 ppm selama 8 jam kerja.
Tingkat iritasi mata: 100 ppm (manusia). Tingkat iritasi mata: 1200 mg / m3 (400 ppm).
Penggunaan
Pelarut organik
Ini adalah pelarut organik yang digunakan untuk melarutkan bromin, yodium dan halogen lainnya; sebagian besar lipid (lemak), resin, karet murni, beberapa alkaloid, gusi, parfum, selulosa asetat, selulosa nitrat, hidrokarbon dan pewarna.
Selain itu, digunakan dalam ekstraksi prinsip-prinsip aktif jaringan hewan dan tanaman, karena memiliki kepadatan yang lebih rendah daripada air dan mengapung di atasnya, meninggalkan zat yang diinginkan larut dalam eter..
Anestesi umum
Ini telah digunakan sebagai anestesi umum sejak 1840, menggantikan kloroform karena memiliki keunggulan terapeutik. Namun, itu adalah zat yang mudah terbakar, dan karena itu, menghadapi kesulitan parah untuk digunakan dalam pengaturan klinis.
Selain itu, itu menghasilkan pada pasien beberapa efek samping pasca operasi yang tidak diinginkan seperti mual dan muntah.
Untuk alasan ini, penggunaan eter sebagai anestesi umum telah dibuang, menggantikannya dengan anestesi lain seperti halotan..
Roh eter
Eter dicampur dengan etanol digunakan untuk membentuk larutan yang disebut semangat eter, digunakan dalam pengobatan perut kembung lambung dan bentuk gastralgia yang lebih ringan.
Evaluasi sirkulasi darah
Eter telah digunakan untuk mengevaluasi sirkulasi darah antara lengan dan paru-paru. Eter disuntikkan ke lengan, membawa darah ke atrium kanan, lalu ke ventrikel kanan dan dari sana ke paru-paru.
Waktu yang berlalu dari injeksi eter, hingga penyerapan bau eter di udara yang dihembuskan, adalah sekitar 4 hingga 6 detik..
Laboratorium pengajaran
Eter digunakan di laboratorium pengajaran dalam banyak percobaan; misalnya, dalam demonstrasi hukum genetika Mendel.
Eter digunakan untuk mematikan lalat dari genus Drosophila dan memungkinkan penyeberangan yang diperlukan di antara mereka, untuk memberikan bukti hukum genetika
Referensi
- Graham Solomons TW., Craig B. Fryhle. (2011). Kimia Organik. Amina (10th edisi.). Wiley Plus.
- Carey F. (2008). Kimia Organik (Edisi keenam). Mc Graw Hill.
- The Sevier. (2018). Dietil eter. Sains Langsung. Diperoleh dari: sciencedirect.com
- Redaksi Encyclopaedia Britannica. (2018). Etil eter. Britannica ncyclopædia. Diperoleh dari: britannica.com
- PubChem (2018). Eter. Diperoleh dari: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Dietil eter. Diperoleh dari: en.wikipedia.org
- Lembar keselamatan XI: etil eter. [PDF] Dipulihkan dari: quimica.unam.mx


