Struktur, sifat, pembentukan, penggunaan asam hidrobromik (HBr)
itu Asam hidrobromik adalah senyawa anorganik yang dihasilkan dari larutan gas yang disebut hidrogen bromida. Rumus kimianya adalah HBr, dan dapat dianggap dengan cara yang berbeda setara: sebagai hidrida molekuler, atau hidrogen halida dalam air; yaitu, hidrazida.
Dalam persamaan kimia, itu harus ditulis sebagai HBr (ac), untuk menunjukkan bahwa itu adalah asam hidrobromik dan bukan gas. Asam ini adalah salah satu yang terkuat, bahkan lebih dari asam klorida, HCl. Penjelasan untuk ini terletak pada sifat ikatan kovalennya.
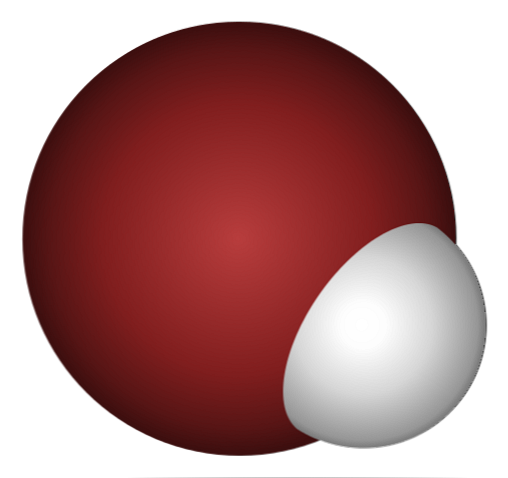
Mengapa HBr bersifat asam, dan bahkan lebih larut dalam air? Karena ikatan kovalen H-Br sangat lemah, karena tumpang tindih yang buruk dari orbital 1s dari H dan 4p dari Br.
Ini tidak mengherankan jika Anda melihat lebih dekat pada gambar di atas, di mana jelas atom brom (coklat) jauh lebih besar daripada atom hidrogen (putih).
Akibatnya, setiap gangguan menyebabkan pemecahan ikatan H-Br, melepaskan ion H+. Kemudian, asam hidrobromik adalah asam Brönsted, karena ia mentransfer proton atau ion hidrogen. Kekuatannya sedemikian rupa sehingga digunakan dalam sintesis beberapa senyawa organobrominasi (seperti 1-Bromo etana, CH3CH2Br).
Asam hidrobromik adalah, setelah hidrik, HI, salah satu hidrosida terkuat dan paling berguna untuk pencernaan sampel padat tertentu.
Indeks
- 1 Struktur asam hidrobromik
- 1.1 Keasaman
- 2 Sifat fisik dan kimia
- 2.1 rumus Molekul
- 2.2 Berat molekul
- 2.3 Penampilan fisik
- 2.4 Bau
- 2.5 Ambang bau
- 2.6 Kepadatan
- 2.7 Titik lebur
- 2.8 Titik didih
- 2.9 Kelarutan dalam air
- 2.10 Kepadatan uap
- 2.11 pK keasaman
- 2.12 Kapasitas kalori
- 2,13 Entalpi molar standar
- 2.14 Entropi molar standar
- 2.15 Titik nyala
- 3 Nomenklatur
- 4 Bagaimana itu terbentuk?
- 4.1 Campuran hidrogen dan bromin dalam air
- 4.2 Fosfor tribromida
- 4.3 Sulfur dioksida dan bromin
- 5 Penggunaan
- 5.1 Persiapan bromida
- 5.2 Sintesis alkil halida
- 5.3 Katalis
- 6 Referensi
Struktur asam hidrobromik
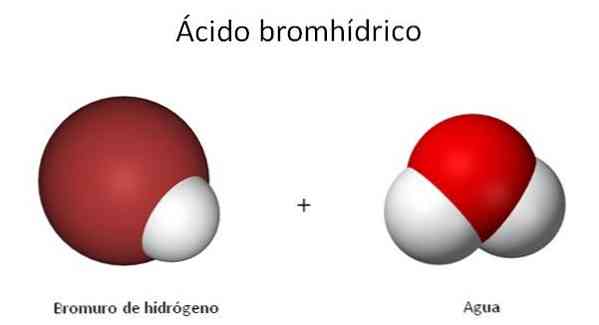
Struktur H-Br diperlihatkan dalam gambar, yang sifat dan karakteristiknya, bahkan gas, terkait erat dengan larutan encernya. Itu sebabnya ada titik di mana Anda masuk ke dalam kebingungan tentang mana dari dua senyawa yang disinggung: HBr atau HBr (ac).
Struktur HBr (ac) berbeda dari HBr, karena sekarang molekul air sedang melarutkan molekul diatomik ini. Ketika cukup dekat, H ditransfer+ ke molekul H2Atau seperti yang ditunjukkan dalam persamaan kimia berikut:
HBr + H2O => Br-- + H3O+
Dengan demikian, struktur asam hidrobromik terdiri dari ion Br-- dan H.3O+ berinteraksi secara elektrostatis. Sekarang, ini sedikit berbeda dari ikatan kovalen H-Br.
Keasamannya yang besar disebabkan oleh anion besar, Br- hampir tidak dapat berinteraksi dengan H3O+, tidak dapat mencegahnya mentransfer H+ untuk spesies kimia lain di sekitarnya.
Keasaman
Misalnya, Cl- dan F- meskipun mereka tidak membentuk ikatan kovalen dengan H3O+, mereka dapat berinteraksi melalui gaya antarmolekul lain, seperti jembatan hidrogen (yang hanya F- dapat menerimanya). Jembatan hidrogen F--H-OH2+ "Hinder" sumbangan H+.
Karena alasan inilah asam hidrofluorat, HF, adalah asam yang lebih lemah dalam air dari asam hidrobromik; sejak itu, interaksi ion Br- H3O+ jangan ganggu pemindahan H+.
Namun, meskipun air hadir dalam HBr (ac), perilakunya pada akhir akun mirip dengan molekul H-Br; yaitu, H+ Ditransfer dari HBr atau Br-H3O+.
Sifat fisik dan kimia
Rumus molekul
HBr.
Berat molekul
80.972 g / mol. Perhatikan bahwa, sebagaimana disebutkan di bagian sebelumnya, hanya HBr yang dipertimbangkan dan bukan molekul air. Jika berat molekul diambil dari rumus Br-H3O+ itu akan memiliki nilai sekitar 99 g / mol.
Penampilan fisik
Cairan kuning tidak berwarna atau pucat, yang akan tergantung pada konsentrasi HBr terlarut. Semakin kuning, semakin terkonsentrasi dan berbahaya.
Bau
Acrid, menjengkelkan.
Ambang bau
6,67 mg / m3.
Kepadatan
1,49 g / cm3 (larutan air pada 48% b / b). Nilai ini, seperti yang sesuai dengan titik leleh dan titik didih, tergantung pada jumlah HBr yang dilarutkan dalam air.
Titik lebur
-11ºC (12ºF, 393ºK) (larutan encer pada 49% b / b).
Titik didih
122 ° C (252 ° F. 393 ° K) pada 700 mmHg (larutan encer 47-49% b / b).
Kelarutan dalam air
-221 g / 100 ml (pada 0 ºC).
-204 g / 100 ml (15 ºC).
-130 g / 100 ml (100 ºC).
Nilai-nilai ini merujuk pada HBr gas, bukan asam hidrobromik. Seperti dapat dilihat, peningkatan suhu menurunkan kelarutan HBr; perilaku yang alami dalam gas. Akibatnya, jika larutan HBr (ac) pekat diperlukan, lebih baik bekerja dengan mereka pada suhu rendah.
Jika bekerja pada suhu tinggi, HBr akan lepas dalam bentuk molekul diatomik gas, sehingga reaktor harus disegel untuk mencegah kebocoran.
Kepadatan uap
2.71 (terkait dengan udara = 1).
Keasaman pKa
-9.0. Konstanta yang sangat negatif ini menunjukkan kekuatan keasamannya yang besar.
Kapasitas kalori
29,1 kJ / mol.
Entalpi molar standar
198,7 kJ / mol (298 ºK).
Entropi molar standar
-36,3 kJ / mol.
Titik penyalaan
Tidak mudah terbakar.
Nomenklatur
Namanya 'asam hidrobromik' menggabungkan dua fakta: keberadaan air, dan bromin yang memiliki valensi -1 dalam senyawa. Dalam bahasa Inggris itu agak lebih jelas: asam hidrobromik, di mana awalan 'hidro' (atau hidro) mengacu pada air; meskipun, sungguh, itu juga bisa merujuk ke hidrogen.
Brom memiliki valensi -1 karena terikat pada atom hidrogen yang kurang elektronegatif daripada itu; tetapi jika dihubungkan atau berinteraksi dengan atom oksigen, ia dapat memiliki banyak valensi, seperti: +2, +3, +5 dan +7. Dengan H hanya dapat mengadopsi valensi tunggal, dan itulah sebabnya akhiran -ico ditambahkan ke namanya.
Sementara HBr (g), hidrogen bromida, bersifat anhidrat; yaitu tidak memiliki air. Oleh karena itu, ia dinamai di bawah standar nomenklatur lain, yang sesuai dengan hidrogen halida.
Bagaimana itu terbentuk?
Ada beberapa metode sintetis untuk menyiapkan asam hidrobromik. Beberapa di antaranya adalah:
Campuran hidrogen dan bromin dalam air
Tanpa menjelaskan rincian teknis, asam ini dapat diperoleh dari campuran langsung hidrogen dan bromin dalam reaktor yang diisi dengan air..
H2 + Br2 => HBr
Dengan cara ini, ketika HBr terbentuk, ia larut dalam air; Ini dapat menyeretnya dalam distilasi, sehingga solusi dapat diekstraksi dengan konsentrasi yang berbeda. Hidrogen adalah gas, dan bromin adalah cairan kemerahan yang gelap.
Fosfor tribromida
Dalam proses yang lebih rumit, pasir, fosfor merah terhidrasi dan bromin dicampur. Perangkap air ditempatkan di penangas es untuk mencegah HBr melarikan diri dan membentuk asam hidrobromik. Reaksinya adalah:
2P + 3Br2 => 2PBr3
PBR3 + 3j2O => 3HBr + H3PO3
Belerang dioksida dan bromin
Cara lain untuk menyiapkannya adalah dengan mereaksikan bromin dengan sulfur dioksida dalam air:
Br2 + SO2 + 2 jam2O => 2HBr + H2SO4
Ini adalah reaksi redoks. Br2 itu mengurangi, ia memperoleh elektron, dengan menghubungkan dengan hidrogen; sedangkan SO2 itu teroksidasi, kehilangan elektron, ketika itu membentuk ikatan kovalen lebih banyak dengan oksigen lain, seperti dalam asam sulfat.
Penggunaan
Persiapan bromida
Garam bromida dapat dibuat jika HBr (ac) bereaksi dengan logam hidroksida. Sebagai contoh, produksi kalsium bromida dipertimbangkan:
Ca (OH)2 + 2HBr => CaBr2 + H2O
Contoh lain adalah untuk natrium bromida:
NaOH + HBr => NaBr + H2O
Dengan demikian, banyak bromida anorganik dapat disiapkan.
Sintesis alkil halida
Dan bagaimana dengan bromida organik? Ini adalah senyawa organobrominasi: RBr atau ArBr.
Dehidrasi alkohol
Bahan baku untuk mendapatkannya bisa berupa alkohol. Ketika diprotonasi dengan keasaman HBr, mereka membentuk air, yang merupakan kelompok keluar yang baik, dan sebaliknya atom tebal Br disatukan, yang akan secara kovalen terkait dengan karbon:
ROH + HBr => RBr + H2O
Dehidrasi ini dilakukan pada suhu di atas 100 ° C, untuk memfasilitasi pecahnya ikatan R-OH2+.
Selain alkena dan alkena
Molekul HBr dapat ditambahkan dari larutannya ke ikatan rangkap atau rangkap tiga atau alkena:
R2C = CR2 + HBr => RHC-CRBr
RC≡CR + HBr => RHC = CRBr
Beberapa produk dapat diperoleh, tetapi dalam kondisi sederhana, produk tersebut pertama kali dibentuk di mana bromin dihubungkan dengan karbon sekunder, tersier atau kuaterner (aturan Markovnikov).
Halida ini campur tangan dalam sintesis senyawa organik lainnya, dan jangkauan penggunaannya sangat luas. Juga, beberapa di antaranya bahkan dapat digunakan dalam sintesis atau desain obat baru.
Clivage Ethereal
Dari eter, dua alkil halida dapat diperoleh secara bersamaan, masing-masing membawa salah satu dari dua rantai samping R atau R 'dari eter awal R-O-R'. Itu terjadi sesuatu yang mirip dengan dehidrasi alkohol, tetapi mekanisme reaksinya berbeda.
Reaksi dapat dirinci dengan persamaan kimia berikut:
ROR '+ 2HBr => RBr + R'Br
Dan air juga dilepaskan.
Katalisator
Keasamannya sedemikian sehingga dapat digunakan sebagai katalis asam yang efektif. Alih-alih menambahkan Br anion- ke struktur molekul, membuka jalan bagi molekul lain untuk melakukannya.
Referensi
- Graham Solomons TW., Craig B. Fryhle. (2011). Kimia Organik. Amina (10th edisi.). Wiley Plus.
- Carey F. (2008). Kimia Organik (Edisi keenam). Mc Graw Hill.
- Steven A. Hardinger. (2017). Illustrated Glossary of Organic Chemistry: Hydrobromic acid. Diperoleh dari: chem.ucla.edu
- Wikipedia. (2018). Asam hidrobromik. Diperoleh dari: en.wikipedia.org
- PubChem. (2018). Asam hidrobromik. Diperoleh dari: pubchem.ncbi.nlm.nih.gov
- Institut Nasional untuk Keselamatan dan Kebersihan di Tempat Kerja. (2011). Hidrogen bromida [PDF] Diperoleh dari: insht.es
- PrepChem. (2016). Persiapan asam hidrobromik. Diperoleh dari: prepchem.com


