Struktur kalsium, bikarbonat, sifat, risiko, dan penggunaan
itu kalsium bikarbonat adalah garam anorganik dengan rumus kimia Ca (HCO)3)2. Itu berasal di alam dari kalsium karbonat hadir dalam batuan kapur dan mineral seperti kalsit.
Kalsium bikarbonat lebih larut dalam air daripada kalsium karbonat. Karakteristik ini memungkinkan pembentukan sistem karst di batuan kapur dan dalam penataan gua.

Perairan bawah tanah yang melewati celah menjadi jenuh dalam perpindahan karbon dioksida (CO2). Perairan ini mengikis batuan kapur melepaskan kalsium karbonat (CaCO3) yang akan membentuk kalsium bikarbonat, sesuai dengan reaksi berikut:
CaCO3+ CO2(g) + H2O (l) => Ca (HCO)3)2(aq)
Reaksi ini terjadi di gua-gua di mana air yang sangat keras berasal. Kalsium bikarbonat tidak ditemukan dalam keadaan padat tetapi dalam larutan encer, bersama dengan Ca2+, bikarbonat (HCO)3-) dan ion karbonat (CO32-).
Selanjutnya, ketika saturasi karbon dioksida dalam air berkurang, reaksi sebaliknya terjadi, yaitu transformasi kalsium bikarbonat menjadi kalsium karbonat:
Ca (HCO)3)2(aq) => CO2 (g) + H2O (l) + CaCO3 (s)
Kalsium karbonat tidak larut dalam air, hal ini menyebabkan pengendapannya terjadi sebagai padatan. Reaksi di atas sangat penting dalam pembentukan stalaktit, stalagmit, dan speleothem lainnya di dalam gua..
Struktur berbatu ini terbentuk dari tetesan air yang jatuh dari langit-langit gua (gambar atas). CaCO3 hadir dalam tetesan air mengkristal untuk membentuk struktur yang disebutkan.
Fakta bahwa kalsium bikarbonat tidak ditemukan dalam keadaan padat membuat penggunaannya sulit, dan beberapa contoh ditemukan. Juga, sulit untuk menemukan informasi tentang efek toksiknya. Ada laporan tentang serangkaian efek samping penggunaannya sebagai pengobatan untuk mencegah osteoporosis.
Struktur
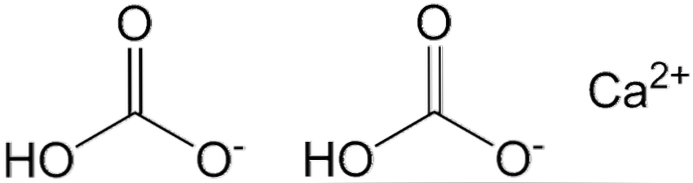
Dua anion HCO ditunjukkan pada gambar atas3- dan kation2+ berinteraksi secara elektrostatis. Ca2+ menurut gambar, itu harus terletak di tengah, karena begitulah HCOs3- mereka tidak akan saling tolak karena tuduhan negatif mereka.
Muatan negatif dalam HCO3- itu terdelokalisasi antara dua atom oksigen, oleh resonansi antara gugus C = O karbonil dan ikatan C-O-; saat di CO32-, Ini terdelokalisasi di antara tiga atom oksigen, karena ikatan C-OH terdeprotonasi dan karenanya dapat menerima muatan negatif melalui resonansi.
Geometri ion-ion ini dapat dianggap sebagai bidang kalsium yang dikelilingi oleh segitiga datar karbonat dengan ujung terhidrogenasi. Dalam hal rasio ukuran, kalsium terasa lebih kecil dari ion HCO3-.
Solusi berair
The Ca (HCO)3)2 Ini tidak dapat membentuk padatan kristal, dan itu benar-benar terdiri dari larutan garam ini. Di dalamnya, ion tidak sendirian, seperti pada gambar, tetapi dikelilingi oleh molekul H.2O.
Bagaimana mereka berinteraksi? Setiap ion dikelilingi oleh bola hidrasi, yang akan tergantung pada logam, polaritas dan struktur spesies terlarut..
Ca2+ berkoordinasi dengan atom oksigen air untuk membentuk aquocomplex, Ca (OH)2)n2+, di mana n umumnya dianggap enam; yaitu, "octahedron berair" di sekitar kalsium.
Sementara anion HCO3- berinteraksi dengan ikatan hidrogen (OR2CO-H-OH2) atau dengan atom hidrogen dalam air searah dengan muatan negatif (HOCO)2- H-OH, interaksi dipol-ion).
Interaksi ini antara Ca2+, HCO3- dan airnya sangat efisien, sehingga membuat kalsium bikarbonat sangat larut dalam pelarut itu; tidak seperti CaCO3, di mana atraksi elektrostatik antara Ca2+ dan CO32- sangat kuat, mengendap dari larutan berair.
Selain air, ada molekul CO2 sekitar, yang bereaksi lambat untuk memberikan lebih banyak HCO3- (tergantung pada nilai pH).
Solid hipotetis
Sejauh ini, ukuran dan muatan ion dalam Ca (HCO)3)2, atau keberadaan air, jelaskan mengapa senyawa padat tidak ada; yaitu, kristal murni yang dapat dikarakterisasi dengan kristalografi sinar-X. Ca (HCO)3)2 tidak lebih dari ion yang ada di dalam air dari mana formasi gua terus tumbuh.
Ya Ca2+ dan HCO3- mereka dapat diisolasi dari air menghindari reaksi kimia berikut:
Ca (HCO)3)2(aq) → CaCO3+ CO2(g) + H2O (l)
Maka ini dapat dikelompokkan dalam padatan kristal putih dengan proporsi stoikiometrik 2: 1 (2HCO3/ 1Ca). Tidak ada penelitian tentang strukturnya, tetapi bisa dibandingkan dengan NaHCO3 (untuk magnesium bikarbonat, Mg (HCO)3)2, tidak ada yang solid), atau dengan CaCO3.
Stabilitas: NaHCO3 vs Ca (HCO)3)2
NaHCO3 mengkristal dalam sistem monoklinik, dan CaCO3 dalam sistem trigonal (kalsit) dan ortorombik (aragonit). Jika Na diganti+ untuk Ca2+, jaringan kristal akan menjadi tidak stabil karena perbedaan ukuran yang lebih besar; yaitu, Na+ karena lebih kecil, ia membentuk kristal yang lebih stabil dengan HCO3- dibandingkan dengan Ca2+.
Bahkan, Ca (HCO)3)2(aq) membutuhkan air untuk menguap sehingga ion-ionnya dapat dikelompokkan dalam kristal; tetapi kisi kristal yang satu ini tidak cukup kuat untuk melakukannya pada suhu kamar. Ketika air dipanaskan, reaksi dekomposisi terjadi (persamaan di atas).
Menjadi ion Na+ dalam larutan, ini akan membentuk kristal dengan HCO3- sebelum dekomposisi termal.
Alasan mengapa Ca (HCO)3)2 itu tidak mengkristal (secara teoritis), itu adalah oleh perbedaan jari-jari ionik atau ukuran ion-ionnya, yang tidak dapat membentuk kristal yang stabil sebelum dekomposisi..
Ca (HCO)3)2 vs CaCO3
Jika di sisi lain, H ditambahkan+ ke struktur kristal CaCO3, mereka akan secara drastis mengubah sifat fisik mereka. Mungkin, titik lelehnya turun drastis, dan bahkan, morfologi kristal akhirnya dimodifikasi.
Apakah ada baiknya mencoba sintesis Ca (HCO)3)2 padat? Kesulitan dapat melebihi harapan, dan garam dengan stabilitas struktural yang rendah mungkin tidak memberikan manfaat tambahan yang signifikan dalam aplikasi apa pun di mana garam lain sudah digunakan.
Sifat fisik dan kimia
Formula kimia
Ca (HCO)3)2
Berat molekul
162.11 g / mol
Keadaan fisik
Itu tidak muncul dalam kondisi padat. Itu ditemukan dalam larutan air dan upaya untuk mengubahnya menjadi padat dengan penguapan air, belum berfungsi karena dikonversi menjadi kalsium karbonat.
Kelarutan dalam air
16,1 g / 100 ml pada 0 ° C; 16,6 g / 100 ml pada 20 ° C dan 18,4 g / 100 ml pada 100 ° C. Nilai-nilai ini menunjukkan afinitas tinggi molekul air untuk ion Ca (HCO)3)2, seperti yang dijelaskan di bagian sebelumnya. Sementara itu, CaCO hanya 15 mg3 mereka larut dalam satu liter air, yang mencerminkan interaksi elektrostatik mereka yang kuat.
Karena Ca (HCO)3)2 tidak dapat membentuk padatan, kelarutannya tidak dapat ditentukan secara eksperimental. Namun, mengingat kondisi yang diciptakan oleh CO2 dilarutkan dalam air yang mengelilingi batu kapur, massa kalsium yang dilarutkan pada suhu T dapat dihitung; massa, yang akan sama dengan konsentrasi Ca (HCO)3)2.
Pada suhu yang berbeda, massa terlarut bertambah seperti yang ditunjukkan oleh nilai pada 0, 20 dan 100 ° C. Jadi, menurut percobaan ini, berapa banyak Ca (HCO) ditentukan3)2 larut di sekitar CaCO3 dalam media berair yang diberi gas dengan CO2. Setelah CO lolos2 gas, CaCO3 akan mengendap, tetapi bukan Ca (HCO3)2.
Fusi dan titik didih
Jaringan kristal Ca (HCO)3)2 jauh lebih lemah dari CaCO3. Jika itu dapat diperoleh dalam keadaan padat, dan mengukur suhu di mana ia mencair di dalam fusiometer, itu pasti akan mendapatkan nilai jauh di bawah 899ºC. Demikian juga, hal yang sama dapat diharapkan dalam penentuan titik didih.
Titik pembakaran
Itu tidak mudah terbakar.
Risiko
Karena senyawa ini tidak ada dalam bentuk padat, kecil kemungkinannya akan mewakili risiko untuk memanipulasi larutan berairnya, karena keduanya2+ sebagai HCO3- mereka tidak berbahaya pada konsentrasi rendah; dan oleh karena itu, risiko terbesar yang akan tertelan solusi seperti itu, bisa disebabkan hanya oleh dosis kalsium yang dikonsumsi yang berbahaya.
Jika senyawa tersebut membentuk padatan, meskipun secara fisik mungkin berbeda dengan CaCO3, efek toksiknya mungkin tidak lebih dari sekadar ketidaknyamanan dan reseksi setelah kontak fisik atau inhalasi.
Penggunaan
-Solusi kalsium bikarbonat telah digunakan sejak lama untuk mencuci kertas bekas, terutama karya seni atau dokumen penting secara historis.
-Penggunaan larutan bikarbonat bermanfaat, tidak hanya karena mereka menetralkan asam dalam kertas, tetapi juga menyediakan cadangan alkali kalsium karbonat. Senyawa terakhir ini memberikan perlindungan terhadap kerusakan di kertas di masa mendatang.
-Seperti bikarbonat lainnya, bikarbonat digunakan dalam ragi kimia dan dalam formulasi tablet atau bubuk effervescent. Selain itu, kalsium bikarbonat digunakan sebagai bahan tambahan makanan (larutan garam ini).
-Solusi bikarbonat telah digunakan dalam pencegahan osteoporosis. Namun, efek sekunder seperti hiperkalsemia, alkalosis metabolik, dan gagal ginjal telah diamati pada satu kasus..
-Kalsium bikarbonat diberikan, kadang-kadang, secara intravena untuk memperbaiki efek depresi hipokalemia pada fungsi jantung.
-Dan akhirnya, ia memberikan kalsium ke tubuh, yang merupakan mediator kontraksi otot, sekaligus memperbaiki asidosis yang dapat terjadi pada kondisi hipokalemia..
Referensi
- Wikipedia. (2018). Kalsium bikarbonat. Diambil dari: en.wikipedia.org
- Sirah Dubois. (3 Oktober 2017). Apa itu Kalsium Bikarbonat? Diperoleh dari: livestrong.com
- Hub Belajar Sains. (2018). Kimia karbonat. Diperoleh dari: sciencelearn.org.nz
- PubChem. (2018). Kalsium Bikarbonat. Diperoleh dari: pubchem.ncbi.nlm.nih.gov
- Amy E. Gerbracht & Irene Brückle. (1997). Penggunaan Solusi Kalsium Bikarbonat dan Magnesium Bikarbonat di Lokakarya Konservasi Kecil: Hasil Survei. Diperoleh dari: cool.conservation-us.org


