Kinerja dan contoh katalis biologis
A katalis biologis o biokatalis adalah molekul, umumnya berasal dari protein, yang memiliki kapasitas untuk mempercepat reaksi kimia yang terjadi di dalam makhluk hidup. Molekul protein katalis adalah enzim, dan yang bersifat RNA adalah ribozim. Dalam artikel ini, kami akan fokus pada eksplorasi enzim, yang merupakan katalis biologis paling terkenal.
Dengan tidak adanya enzim, sejumlah besar reaksi yang terjadi di dalam sel dan yang memungkinkan kehidupan, tidak dapat terjadi. Ini bertanggung jawab untuk mempercepat proses dalam urutan besarnya mendekati 106 - dan dalam beberapa kasus jauh lebih besar.
Indeks
- 1 Katalisis
- 2 Enzim
- 2.1 Apa itu enzim?
- 2.2 Karakteristik enzim
- 2.3 Nomenklatur dan klasifikasi enzim
- 2.4 Bagaimana enzim bekerja?
- 2.5 Inhibitor enzimatik
- 2.6 Contoh
- 3 Perbedaan antara katalis biologis (enzim) dan katalis kimia
- 3.1 Reaksi yang dikatalisis oleh enzim terjadi lebih cepat
- 3.2 Sebagian besar enzim bekerja pada kondisi fisiologis
- 3.3 Kekhususan
- 3.4 Regulasi enzimatik akurat
- 4 Referensi
Katalisis
Katalis adalah molekul yang mampu mengubah kecepatan reaksi kimia tanpa dikonsumsi dalam reaksi tersebut.
Reaksi kimia melibatkan energi: molekul awal yang terlibat dalam reaksi atau reaktan dimulai dengan tingkat energi. Sejumlah tambahan energi diserap untuk mencapai "keadaan transisi". Selanjutnya, energi dilepaskan bersama produk.
Perbedaan energi antara reaktan dan produk dinyatakan sebagai ΔG. Jika tingkat energi produk lebih besar dari reaktan, reaksinya bersifat endergonik dan tidak spontan. Sebaliknya, jika energi produk lebih rendah, reaksinya bersifat eksergonik dan spontan.
Namun, jika suatu reaksi spontan, itu tidak berarti bahwa itu akan terjadi pada kecepatan yang cukup besar. Kecepatan reaksi tergantung pada ΔG * (tanda bintang mengacu pada energi aktivasi).
Pembaca harus mengingat konsep-konsep ini dalam rangka untuk memahami bagaimana fungsi enzim terjadi.
Enzim
Apa itu enzim?
Enzim adalah molekul biologis dengan kompleksitas luar biasa, terutama terdiri dari protein. Protein, pada gilirannya, adalah rantai panjang asam amino.
Salah satu karakteristik enzim yang paling menonjol adalah spesifisitasnya dalam molekul target - molekul ini disebut substrat.
Karakteristik enzim
Enzim ada dalam beberapa bentuk. Beberapa seluruhnya terdiri dari protein, sementara yang lain memiliki daerah non-protein yang disebut kofaktor (logam, ion, molekul organik, dll.).
Jadi, suatu apoenzim adalah enzim tanpa kofaktornya, dan kombinasi dari apoenzim dan kofaktornya disebut holoenzim.
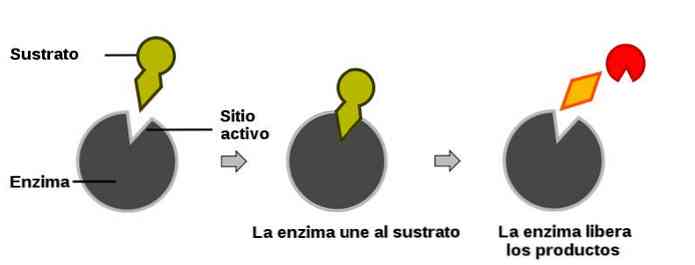
Mereka adalah molekul dengan ukuran yang sangat besar. Namun, hanya situs kecil enzim yang secara langsung berpartisipasi dalam reaksi dengan substrat, dan wilayah ini adalah situs aktif.
Ketika reaksi dimulai, enzim digabungkan dengan substratnya ketika sebuah kunci digabungkan dengan kuncinya (model ini adalah penyederhanaan proses biologis yang sebenarnya, tetapi berfungsi untuk menggambarkan proses tersebut).
Semua reaksi kimia yang terjadi dalam tubuh kita dikatalisis oleh enzim. Faktanya, jika molekul-molekul ini tidak ada, kita harus menunggu ratusan atau ribuan tahun untuk menyelesaikannya. Karena itu, pengaturan aktivitas enzimatik harus dikontrol dengan cara yang sangat spesifik.
Nomenklatur dan klasifikasi enzim
Ketika kita melihat molekul yang namanya berakhiran -ase, kita dapat yakin bahwa itu adalah enzim (walaupun ada pengecualian untuk aturan ini, seperti trypsin). Ini adalah konvensi untuk menunjuk nama enzim.
Ada enam tipe dasar enzim: oksidoreduktase, transferase, hidrolase, lyase, isomerase dan ligase; bertanggung jawab untuk: reaksi redoks, transfer atom, hidrolisis, penambahan ikatan rangkap, isomerisasi dan pengikatan molekul, masing-masing.
Bagaimana enzim bekerja?
Pada bagian katalisis, kami menyebutkan bahwa kecepatan reaksi tergantung pada nilai ΔG *. Semakin tinggi nilai ini, semakin lambat dan semakin lambat pula reaksinya. Enzim ini bertanggung jawab untuk mengurangi parameter tersebut - sehingga meningkatkan kecepatan reaksi.
Perbedaan antara produk dan reaktan tetap identik (enzim tidak mempengaruhinya), seperti halnya distribusi yang sama. Enzim memfasilitasi pembentukan keadaan transisi.
Inhibitor enzim
Dalam konteks studi tentang enzim, inhibitor adalah zat yang berhasil menurunkan aktivitas katalis. Mereka diklasifikasikan menjadi dua jenis: inhibitor kompetitif dan non-kompetitif. Mereka yang dari jenis pertama bersaing dengan substrat dan yang lainnya tidak.
Umumnya proses penghambatan bersifat reversibel, meskipun beberapa inhibitor dapat tetap digabungkan ke enzim hampir secara permanen.
Contohnya
Ada sejumlah besar enzim di dalam sel kita - dan di dalam sel semua makhluk hidup. Namun, yang paling terkenal adalah mereka yang berpartisipasi dalam jalur metabolisme seperti glikolisis, siklus Krebs, rantai transpor elektron, antara lain..
Succinate dehydrogenase adalah enzim tipe oksidoreduktase yang mengkatalisasi oksidasi suksinat. Dalam hal ini, reaksi melibatkan hilangnya dua atom hidrogen.
Perbedaan antara katalis biologis (enzim) dan katalis kimia
Ada katalis yang bersifat kimia yang, seperti yang biologis, meningkatkan kecepatan reaksi. Namun, ada perbedaan penting antara kedua jenis molekul.
Reaksi yang dikatalisis oleh enzim terjadi lebih cepat
Pertama, enzim berhasil meningkatkan kecepatan reaksi dengan urutan mendekati 106 hingga 1012. Katalis kimia juga meningkatkan kecepatan, tetapi hanya beberapa urutan besarnya.
Sebagian besar enzim bekerja pada kondisi fisiologis
Ketika reaksi biologis dilakukan di dalam makhluk hidup, kondisi optimalnya mengelilingi nilai-nilai fisiologis suhu dan pH. Ahli kimia, di sisi lain, membutuhkan kondisi suhu, tekanan, dan keasaman yang drastis.
Kekhususan
Enzim sangat spesifik dalam reaksi yang dikatalisasi. Dalam kebanyakan kasus, mereka hanya bekerja dengan satu media atau dengan sedikit media. Kekhususan juga berlaku untuk jenis produk yang mereka hasilkan. Kisaran substrat katalis kimia jauh lebih luas.
Kekuatan yang menentukan kekhususan interaksi antara enzim dan substratnya adalah sama yang menentukan konformasi protein yang sama (interaksi Van der Waals, elektrostatik, ikatan hidrogen, dan hidrofobik).
Regulasi enzimatiknya tepat
Akhirnya, enzim memiliki kapasitas regulasi yang lebih besar dan aktivitasnya bervariasi sesuai dengan konsentrasi berbagai zat dalam sel.
Di antara mekanisme pengaturan kami menemukan kontrol alosterik, modifikasi kovalen enzim dan variasi jumlah enzim yang disintesis.
Referensi
- Berg, J. M., Stryer, L., & Tymoczko, J. L. (2007). Biokimia. Saya terbalik.
- Campbell, M. K., & Farrell, S. O. (2011). Biokimia Edisi keenam. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Buku teks biokimia. John Wiley & Sons.
- Koolman, J., & Röhm, K. H. (2005). Biokimia: teks dan atlas. Ed. Panamericana Medical.
- Mougios, V. (2006). Latihan biokimia. Kinetika Manusia.
- Müller-Esterl, W. (2008). Biokimia Dasar-dasar untuk ilmu kedokteran dan kehidupan. Saya terbalik.
- Poortmans, J.R. (2004). Prinsip latihan biokimia. Lebih besar.
- Voet, D., & Voet, J. G. (2006). Biokimia. Ed. Panamericana Medical.


