Ammonium Sulfat, Struktur Kimia, Properti dan Penggunaan
itu amonium sulfat Ini adalah garam anorganik asam sulfat terner dan amoniak. Formula kimianya adalah (NH4)2SO4. Oleh karena itu, proporsi stoikiometrik mengatakan bahwa untuk setiap anion sulfat ada dua kation amonium yang berinteraksi dengannya. Ini memungkinkan netralitas garam ((+1) ∙ 2 + (-2)).
Nomenklaturanya disebabkan oleh fakta bahwa itu adalah garam yang berasal dari H2SO4, mengubah akhiran "uric" menjadi "ato". Dengan demikian, dua proton awal digantikan oleh NH4+, produk reaksi dengan amonia (NH3). Kemudian, persamaan kimia untuk sintesisnya adalah: 2 NH3 + H2SO4 => (NH4)2SO4
Amonium sulfat adalah simpanan nitrogen dan belerang, keduanya sangat diperlukan dalam kimia tanah dan pupuk.
Indeks
- 1 Struktur kimia
- 2 Sifat fisik dan kimia
- 2.1 Berat molekul
- 2.2 Penampilan fisik
- 2.3 Bau
- 2.4 Titik lebur
- 2.5 Kelarutan
- 2.6 Kepadatan
- 2.7 Tekanan uap
- 2.8 Titik nyala
- 2,9 pH
- 2.10 Stabilitas
- 2.11 Penguraian
- 2.12 Korosi
- 3 Penggunaan
- 3.1 Di bidang pertanian
- 3.2 Sebagai reagen analitis
- 3.3 Dalam pengendapan dan isolasi protein
- 3.4 Di industri
- 3.5 Penggunaan lainnya
- 4 Referensi
Struktur kimia
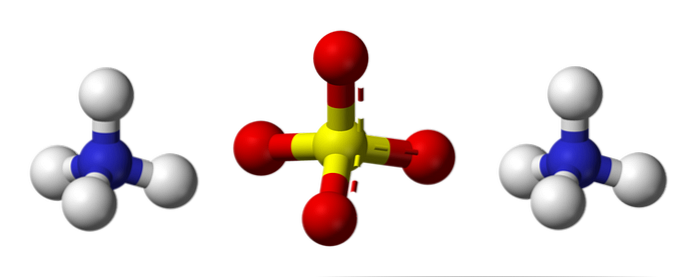
Gambar atas menggambarkan geometri molekul ion NH4+ dan SO42-. Bola merah sesuai dengan atom oksigen, bola putih sesuai dengan atom hidrogen, bola biru dengan atom nitrogen dan bola kuning sesuai dengan atom belerang.
Kedua ion dapat dianggap sebagai dua tetrahedron, sehingga memiliki tiga unit yang berinteraksi membentuk susunan kristal ortorombik. Anion sulfat adalah SO42- dan mampu menyumbangkan atau menerima empat ikatan hidrogen, seperti kation NH4+.
Sifat fisik dan kimia
Berat molekul
132.134 g / mol.
Penampilan fisik
Putih pekat. Kristal putih atau coklat ortorombik, tergantung pada tingkat pengotornya.
Bau
Toilet.
Titik lebur
280 ºC. Titik lebur ini, rendah dibandingkan dengan senyawa ionik lainnya, disebabkan oleh fakta bahwa itu adalah garam dengan kation monovalen (+1) dan dengan ion yang berbeda dalam ukurannya, menyebabkan padatan memiliki energi reticular kristal rendah.
Kelarutan
76,4 g / 100 g air pada 25 ºC. Afinitas terhadap air ini disebabkan oleh kapasitas molekulnya yang besar untuk melarutkan ion amonium. Di sisi lain, tidak larut dalam aseton dan alkohol; yaitu, dalam pelarut lebih sedikit polar daripada air.
Kepadatan
1,77 g / cm3 pada 25 ºC.
Tekanan uap
1.871 kPa pada 20 ºC.
Titik mudah terbakar
26 ºC.
pH
5.0-6.0 (25 ° C, solusi 1 M). PH yang sedikit asam disebabkan oleh hidrolisis NH4+ dalam air, menghasilkan H3O+ pada konsentrasi rendah.
Stabilitas
Stabil dalam kondisi lingkungan yang sesuai. Jika kontak dengan oksidan kuat dapat terbakar.
Dekomposisi
Itu mulai terurai pada 150 ºC, melepaskan uap beracun dari sulfur oksida, nitrogen oksida dan amonium.
Korosi
Tidak menyerang besi atau aluminium.
Penggunaan

Di bidang pertanian
- Amonium sulfat digunakan sebagai pupuk di tanah alkali. Garam amonium memiliki 21% nitrogen dan 24% sulfur dalam komposisinya. Namun, ada senyawa yang memberikan jumlah nitrogen lebih besar daripada amonium sulfat; Keuntungan dari yang terakhir adalah konsentrasi belerang yang tinggi.
- Belerang sangat penting dalam sintesis protein, karena beberapa asam amino - seperti sistin, metionin, dan sistein - memiliki sulfur. Karena alasan ini, amonium sulfat terus menjadi salah satu pupuk terpenting.
- Ini digunakan dalam tanaman gandum, jagung, beras, kapas, kentang, rami dan pohon buah.
- Tanah alkali pH rendah karena kontribusinya terhadap proses nitrifikasi yang dilakukan oleh mikroba. Amonium (NH) digunakan4+) untuk menghasilkan nitrat (NO3-) dan lepaskan H+: 2NH4+ + 4O2 => 2NO3- + 2 jam2O + 4H+. Peningkatan konsentrasi hidrogen menurunkan pH tanah alkali dan memungkinkan lebih banyak digunakan.
- Selain penggunaannya sebagai pupuk, amonium sulfat bertindak sebagai coadjuvant untuk insektisida terlarut, herbisida dan fungisida, yang disemprotkan ke tanaman..
- Sulfat mampu menyerap ion yang ada di tanah dan air irigasi yang diperlukan untuk kehidupan patogen tertentu. Di antara ion-ion yang ditangkap oleh ammonium sulfat adalah Ca2+, Mg2+, Iman2+ dan Iman3+. Tindakan ini meningkatkan efek mikrobisida dari agen yang disebutkan.
Sebagai reagen analitis
Amonium sulfat bertindak sebagai zat pengendap dalam analisis elektrokimia, dalam media kultur mikrobiologis dan dalam pembuatan garam amonium.
Dalam presipitasi dan isolasi protein
Amonium sulfat digunakan dalam isolasi dan pemurnian protein, terutama protein plasma. Sejumlah amonium sulfat ditambahkan ke plasma pada konsentrasi tertentu; dengan demikian, pengendapan sekelompok protein disebabkan.
Endapan dikumpulkan dengan sentrifugasi dan sejumlah tambahan amonium sulfat ditambahkan ke supernatan dan, pada konsentrasi baru, pengendapan kelompok protein lain terjadi..
Pengulangan proses sebelumnya dalam bentuk sekuensial memungkinkan mendapatkan fraksi protein plasma yang berbeda sebagai hasilnya.
Sebelum muncul teknologi baru biologi molekuler, prosedur ini memungkinkan isolasi protein plasma yang sangat penting dalam kedokteran, misalnya: imunoglobulin, faktor koagulasi, dll..
Dalam industri
Ammonium sulfate bertindak untuk memperlambat dimulainya kebakaran di industri tekstil. Ini digunakan sebagai aditif dalam industri elektroplating. Ini juga digunakan dalam produksi hidrogen peroksida, amonium klorida, dll..
Penggunaan lainnya
- Amonium sulfat digunakan sebagai zat pengatur tekanan osmotik dan sebagai zat pengendap garam.
- Dalam bentuk amonium lauril sulfat, tegangan permukaan air berkurang, sehingga memungkinkan pemisahan polutan dengan meningkatkan kekerasan air..
- Ini adalah agen anti korosi.
- Ini digunakan sebagai aditif makanan yang mengatur keasaman dalam adonan tepung dan roti.
Referensi
- SIDS OECD. (Oktober 2004). Amonium sulfat. [PDF] Diperoleh pada 27 April 2018, dari: inchem.org
- Perusahaan Mosaik. (2018). Amonium sulfat. Diperoleh pada 27 April 2018, dari: cropnutrition.com
- Wikipedia. (2018). Amonium sulfat. Diperoleh pada 27 April 2018, dari: en.wikipedia.org
- Pubchem. (2018). Amonium sulfat. Diperoleh pada 27 April 2018, dari: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 Juli 2015). [Gambar] Diperoleh pada 27 April 2018, dari: flickr.com
- Paula Papp (22 Februari 2017). Aplikasi dan penggunaan amonium sulfat. Diperoleh pada 27 April 2018, dari: business.com


