Radius atom bagaimana diukur, bagaimana ia berubah dalam tabel periodik, contoh
itu jari-jari atom ini adalah parameter penting untuk properti periodik elemen tabel periodik. Ini terkait langsung dengan ukuran atom, karena pada radius yang lebih besar, lebih besar atau besar. Demikian juga, itu terkait dengan karakteristik elektronik yang sama.
Selama atom memiliki lebih banyak elektron, semakin besar ukurannya dan jari-jari atomnya. Keduanya ditentukan oleh elektron dari kulit valensi, karena pada jarak di luar orbitnya, probabilitas menemukan elektron mendekati nol. Kebalikannya terjadi di sekitar inti: probabilitas menemukan elektron meningkat.

Gambar atas merupakan kemasan bola kapas. Perhatikan bahwa masing-masing dikelilingi oleh enam tetangga, tanpa menghitung kemungkinan baris atas atau bawah lainnya. Cara bola kapas dipadatkan akan menentukan ukurannya dan, karenanya, jari-jarinya; seperti halnya dengan atom.
Unsur-unsur sesuai dengan sifat kimianya berinteraksi dengan atom mereka sendiri dengan satu atau lain cara. Oleh karena itu, besarnya jari-jari atom bervariasi sesuai dengan jenis ikatan yang ada dan pengemasan padat atom-atomnya.
Indeks
- 1 Bagaimana jari-jari atom diukur?
- 1.1 Penentuan jarak internuklear
- 1.2 Unit
- 2 Bagaimana perubahan dalam tabel periodik?
- 2.1 Selama periode
- 2.2 Turun menurut kelompok
- 2.3 Kontraksi lantanida
- 3 Contoh
- 4 Referensi
Bagaimana jari-jari atom diukur?
Pada gambar utama, bisa dengan mudah mengukur diameter bola kapas, dan kemudian membaginya menjadi dua. Namun, bola atom tidak sepenuhnya ditentukan. Mengapa Karena elektron bersirkulasi dan berdifusi di wilayah ruang tertentu: orbital.
Oleh karena itu, atom dapat dianggap sebagai bola dengan tepi yang tidak dapat ditembus, yang tidak mungkin dikatakan dengan pasti sampai sejauh mana mereka berakhir. Misalnya, pada gambar atas wilayah tengah, dekat nukleus, terlihat warna yang lebih pekat, sedangkan tepinya kabur.
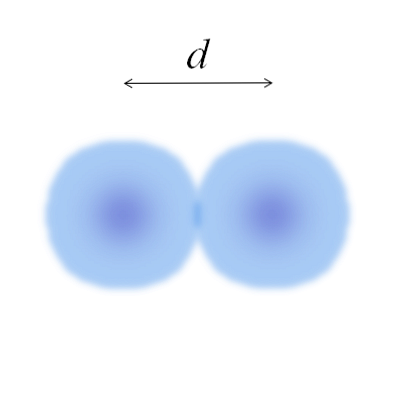
Gambar tersebut mewakili molekul diatomik E2 (sebagai Cl2, H2, O2, dll.) Dengan asumsi bahwa atom adalah benda bulat, jika jaraknya ditentukan d yang memisahkan kedua inti dalam ikatan kovalen, maka itu akan cukup untuk membaginya menjadi dua bagian (d/ 2) untuk mendapatkan jari-jari atom; lebih tepatnya, jari-jari kovalen E untuk E2.
Dan jika E tidak membentuk ikatan kovalen dengan dirinya sendiri, tetapi itu adalah unsur logam? Lalu d itu akan ditunjukkan oleh jumlah tetangga yang mengelilingi E dalam struktur logamnya; yaitu, dengan nomor koordinasi (N.C) atom dalam kemasan (ingat bola kapas dari gambar utama).
Penentuan jarak internuclear
Untuk menentukan d, yang merupakan jarak internuklear untuk dua atom dalam molekul atau kemasan, itu membutuhkan teknik analisis fisik.
Salah satu yang paling umum digunakan adalah difraksi sinar-X. Di dalamnya sinar cahaya disinari melalui kristal, dan pola difraksi yang dihasilkan dari interaksi antara elektron dan radiasi elektromagnetik dipelajari. Tergantung pada pengepakan, pola difraksi yang berbeda dapat diperoleh dan, karenanya, nilai lain dari d.
Jika atom "kencang" dalam kisi kristal, mereka akan memberikan nilai yang berbeda d dibandingkan dengan apa yang akan mereka miliki jika mereka "nyaman". Juga, jarak-jarak internuklear ini dapat berosilasi dalam nilai-nilai, sehingga jari-jari atom sebenarnya terdiri dari nilai rata-rata dari pengukuran tersebut.
Bagaimana jari-jari atom dan nomor koordinasi terkait? V. Goldschmidt menjalin hubungan antara keduanya, di mana untuk NC dari 12, nilai relatif adalah 1; dari 0,97 untuk kemasan di mana atom memiliki NC sama dengan 8; 0,96, untuk N.C sama dengan 6; dan 0,88 untuk N.C 4.
Unit
Dari nilai untuk N.C sama dengan 12, banyak tabel telah dibangun membandingkan jari-jari atom semua elemen dari tabel periodik.
Karena tidak semua elemen membentuk struktur kompak seperti itu (N.C kurang dari 12), hubungan V. Goldschmidt digunakan untuk menghitung jari-jari atom mereka dan mengekspresikannya untuk kemasan yang sama. Dengan cara ini, pengukuran jari-jari atom distandarisasi.
Tetapi dalam unit apa mereka mengekspresikan diri? Sejak d besarnya sangat kecil, harus menggunakan unit angstrom Å (10 ∙ 10-10m) atau juga banyak digunakan, pikometer (10 ∙ 10-12m).
Bagaimana cara mengubahnya dalam tabel periodik?
Sepanjang periode
Jari-jari atom ditentukan untuk elemen logam diberi nama jari-jari logam, sedangkan untuk elemen non-logam, jari-jari kovalen (seperti fosfor, P4, atau belerang, S8). Namun, antara kedua jenis radio ada perbedaan yang lebih menonjol dari namanya.
Dari kiri ke kanan pada periode yang sama, nukleus menambahkan proton dan elektron, tetapi yang terakhir terbatas pada tingkat energi yang sama (nomor kuantum utama). Sebagai konsekuensinya, nukleus mengerahkan muatan nuklir efektif yang meningkat pada elektron valensi, yang berkontraksi dengan jari-jari atom.
Dengan cara ini, unsur-unsur non-logam pada periode yang sama cenderung memiliki jari-jari atom (kovalen) lebih kecil dari logam (jari-jari logam).
Turun menurut kelompok
Ketika turun oleh suatu kelompok, tingkat energi baru diaktifkan, yang memungkinkan elektron memiliki lebih banyak ruang. Dengan demikian, awan elektronik mencakup jarak yang lebih jauh, pinggirannya yang kabur akhirnya bergerak menjauh dari nukleus, dan karenanya, jari-jari atom mengembang.
Kontraksi lantanida
Elektron pada lapisan dalam membantu melindungi muatan nuklir efektif pada elektron valensi. Ketika orbital yang membentuk lapisan dalam memiliki banyak "lubang" (node), seperti halnya orbital f, nukleus berkontraksi dengan kuat jari-jari atom karena efek perlindungan yang buruk dari orbital..
Fakta ini dibuktikan dalam kontraksi lantanida pada periode 6 tabel periodik. Dari La ke Hf ada kontraksi yang cukup besar dari jari-jari atom yang dihasilkan oleh orbital f, yang "terisi" ketika seseorang melewati blok f: lantanoid dan actinoid.
Efek serupa juga dapat diamati dengan unsur-unsur blok p dari periode 4. Produk kali ini dari efek perisai lemah orbital d yang terisi ketika melintasi periode logam transisi.
Contohnya
Untuk periode 2 tabel periodik, jari-jari atom unsur-unsurnya adalah:
-Li: 257 siang
-Jadilah: 112 siang
-B: 88 malam
-C: 77 sore
-N: 74 sore
-O: 66 sore
-F: 64 p.m.
Perhatikan bahwa logam lithium memiliki jari-jari atom terbesar (257 hal), sedangkan fluor, yang terletak di ujung kanan periode, adalah yang terkecil dari mereka (64 hal). Jari-jari atom turun dari kiri ke kanan pada periode yang sama, dan nilai-nilai yang tercantum menunjukkannya.
Lithium, dengan membentuk ikatan logam, jari-jarinya adalah logam; dan fluorin, karena membentuk ikatan kovalen (F-F), jari-jarinya kovalen.
Dan jika Anda ingin mengekspresikan radio atom dalam satuan angstrom? Cukup bagi dengan 100: (257/100) = 2.57Å. Demikian seterusnya dengan nilai-nilai lainnya.
Referensi
- Kimia 301. Radius Atom. Diperoleh dari: ch301.cm.utexas.edu
- Yayasan CK-12. (28 Juni 2016). Radius Atom. Diperoleh dari: chem.libretexts.org
- Tren dalam Radius Atom. Diambil dari: intro.chem.okstate.edu
- Clackamas Community College. (2002). Ukuran Atom. Diperoleh dari: dl.clackamas.edu
- Clark J. (Agustus 2012). Radius Atom dan Ionik. Diperoleh dari: chemguide.co.uk
- Menggigil & Atkins. (2008). Kimia anorganik (Edisi keempat., Hal 23, 24, 80, 169). Mc Graw Hill.


