Hukum sejarah Boyle-Mariotte, ekspresi matematika, contoh-contoh
Hukum Boyle-Mariotte adalah apa yang mengekspresikan hubungan antara tekanan yang diberikan oleh atau pada gas, dan volume yang ditempati olehnya; menjaga konstan suhu gas, serta kuantitasnya (jumlah mol).
Hukum ini, bersama dengan Charles, Gay-Lussac, Charles dan Avogadro, menggambarkan perilaku gas ideal; khususnya, dalam wadah tertutup yang tunduk pada perubahan volume yang diberikan oleh gaya mekanis.
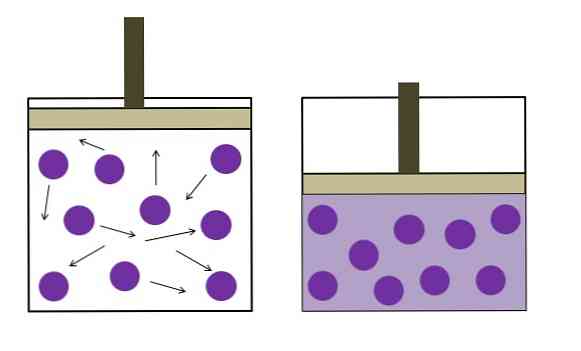
Gambar di atas secara singkat merangkum hukum Boyle-Mariotte.
Titik-titik ungu mewakili molekul atau atom gas, yang bertabrakan dengan dinding bagian dalam wadah (kiri). Dengan mengurangi ruang yang tersedia atau volume wadah yang ditempati oleh gas ini, tumbukan meningkat, yang berarti peningkatan tekanan (kanan).
Ini menunjukkan bahwa tekanan P dan volume V gas berbanding terbalik jika wadah tertutup rapat; jika tidak, tekanan yang lebih tinggi akan sama dengan ekspansi wadah yang lebih besar.
Jika plot V dibuat terhadap P, dengan data V dan P pada sumbu Y dan X, masing-masing, kurva asimtotik akan diamati. Semakin kecil V, semakin besar peningkatan P; yaitu, kurva akan meluas ke nilai P yang tinggi pada sumbu X.
Tentu saja, suhunya tetap konstan; tetapi, jika percobaan yang sama dilakukan pada suhu yang berbeda, posisi relatif dari kurva V vs P ini akan berubah pada sumbu Cartesian. Perubahan akan lebih jelas jika diplot pada sumbu tiga dimensi, dengan T konstan pada sumbu Z.
Indeks
- 1 Sejarah hukum Boyle
- 1.1 Latar Belakang
- 1.2 Percobaan dengan merkuri
- 1.3 Edme Mariotte
- 1.4 Memperkuat hukum
- 2 Terdiri dari apakah undang-undang ini??
- 3 Ekspresi matematis
- 4 Untuk apa ini? Masalah apa yang dipecahkan oleh hukum Boyle??
- 4.1 Mesin uap
- 4.2 Menghirup minuman
- 4.3 Sistem pernapasan
- 5 Contoh (percobaan)
- 5.1 Eksperimen 1
- 5.2 Eksperimen 2
- 6 Referensi
Sejarah hukum Boyle
Latar belakang
Karena ilmuwan Galileo Galilei menyatakan keyakinannya pada keberadaan kekosongan (1638), para ilmuwan mulai mempelajari sifat-sifat lubang udara dan parsial.
Ahli kimia Anglo-Irlandia, Robert Boyle, memulai studinya tentang sifat-sifat udara pada tahun 1638 setelah mengetahui bahwa Otto von Guericke, seorang insinyur dan ahli fisika Jerman, telah membangun sebuah pompa udara..
Percobaan dengan merkuri
Untuk melakukan penelitian tentang tekanan udara, Boyle menggunakan tabung kaca dalam bentuk "J", yang konstruksinya dikaitkan dengan Robert Hooke, asisten Boyle. Ujung lengan pendek disegel, sedangkan ujung lengan panjang tabung terbuka untuk menempatkan merkuri.
Sejak awal, Boyle ingin mempelajari elastisitas udara, secara kualitatif dan kuantitatif. Dengan menuangkan merkuri melalui ujung terbuka tabung berbentuk "J", Boyle menyimpulkan bahwa udara di lengan pendek tabung itu berkontraksi di bawah tekanan merkuri..
Hasil
Semakin besar jumlah merkuri yang ditambahkan ke tabung, semakin besar tekanan yang diberikan di udara dan semakin rendah volumenya. Boyle memperoleh grafik tipe eksponensial negatif dari volume udara sebagai fungsi tekanan.
Sementara, jika Anda memplot volume udara terhadap tekanan terbalik, Anda memiliki garis lurus kemiringan positif.
Pada 1662, Boyle menerbitkan hukum fisika pertama yang diberikan dalam bentuk persamaan, yang menunjukkan ketergantungan fungsional dua variabel. Dalam hal ini, tekanan dan volumenya.
Boyle menunjukkan bahwa ada hubungan terbalik antara tekanan yang diberikan pada gas dan volume yang ditempati oleh gas itu, rasio ini relatif benar untuk gas nyata. Sebagian besar gas berperilaku seperti gas ideal pada tekanan dan suhu sedang.
Dengan tekanan yang lebih tinggi dan suhu yang lebih rendah, penyimpangan dari perilaku gas nyata dari cita-cita menjadi lebih nyata.
Edme Mariotte
Fisikawan Perancis Edme Mariotte (1620-1684) secara independen menemukan hukum yang sama pada tahun 1679. Tetapi ia pantas menunjukkan bahwa volumenya bervariasi sesuai suhu. Karena itulah disebut Hukum Mariotte atau Hukum Boyle dan Mariotte.
Memperkuat hukum
Daniel Bernoulli (1737) memperkuat Hukum Boyle dengan menunjukkan bahwa tekanan gas dihasilkan oleh dampak partikel gas pada dinding wadah yang mengandungnya..
Pada tahun 1845, John Waterston menerbitkan sebuah artikel ilmiah, di mana ia berfokus pada prinsip-prinsip utama teori kinetik gas.
Kemudian, Rudolf Clausius, James Maxwell dan Ludqwig Boltzmann mengkonsolidasikan teori kinetik gas, yang menghubungkan tekanan yang diberikan oleh gas dengan kecepatan partikel-partikel gas yang bergerak..
Semakin kecil volume wadah berisi gas, semakin besar frekuensi dampak partikel yang membentuknya terhadap dinding wadah; dan karena itu, semakin besar tekanan yang diberikan oleh gas.
Terdiri dari apa undang-undang ini??
Eksperimen yang dilakukan oleh Boyle menunjukkan bahwa ada hubungan terbalik antara volume yang ditempati oleh gas dan tekanan yang diberikan padanya. Namun, hubungan tersebut tidak sepenuhnya linier, seperti yang ditunjukkan oleh grafik variasi volume sesuai dengan tekanan yang dikaitkan dengan Boyle.
Dalam Hukum Boyle ditunjukkan bahwa volume yang ditempati oleh gas berbanding terbalik dengan tekanan. Juga diindikasikan bahwa produk tekanan gas dengan volumenya konstan.
Ekspresi matematis
Untuk sampai pada ekspresi matematis hukum Boyle-Mariotte, kita mulai dari:
V α 1 / P
Di mana itu menunjukkan bahwa volume yang ditempati oleh gas berbanding terbalik dengan tekanannya. Namun, ada konstanta yang menentukan seberapa berbanding terbalik hubungan ini.
V = k / P
Di mana k adalah konstanta proporsionalitas. Kliring k yang Anda miliki:
VP = k
Produk tekanan gas dengan volumenya konstan. Lalu:
V1P1 = k dan V2P2 = k
Dan dari sini dapat disimpulkan bahwa:
V1P1 = V2P2
Yang terakhir adalah ungkapan atau persamaan terakhir untuk hukum Boyle.
Untuk apa ini? Masalah apa yang dipecahkan oleh hukum Boyle??
Mesin uap

Hukum Boyle-Mariotte berlaku untuk pengoperasian mesin uap. Ini adalah mesin pembakaran eksternal yang menggunakan transformasi energi termal dari sejumlah air menjadi energi mekanik.
Air dipanaskan dalam boiler yang tertutup rapat, dan uap yang dihasilkan memberikan tekanan sesuai dengan hukum Boyle-Mariote yang menghasilkan ekspansi volume silinder dengan mendorong piston.
Gerakan linear piston diubah menjadi gerakan rotasi, melalui penggunaan sistem engkol dan engkol, yang dapat menggerakkan roda lokomotif atau rotor generator listrik..
Saat ini, mesin uap alternatif adalah mesin yang sedikit digunakan, karena telah digantikan oleh motor listrik dan mesin pembakaran internal pada kendaraan angkut..
Menghirup minuman
Tindakan mengisap minuman ringan atau jus dari botol melalui tabung plastik terkait dengan hukum Boyle-Mariotte. Ketika udara dihisap dari tabung menggunakan mulut, ada penurunan tekanan di dalam tabung.
Penurunan tekanan ini memfasilitasi gerakan ke atas cairan dalam tabung, memungkinkan tertelannya. Prinsip yang sama ini bekerja dalam ekstraksi darah dengan menggunakan jarum suntik.
Sistem pernapasan
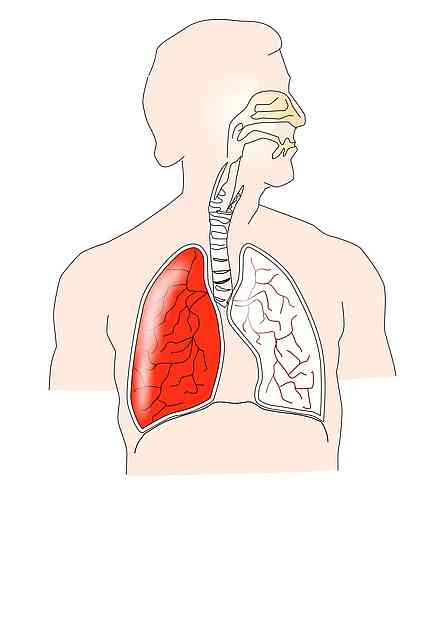
Hukum Boyle-Mariotte terkait erat dengan fungsi sistem pernapasan. Selama fase inspirasi, kontraksi diafragma dan otot lainnya terjadi; misalnya, intercostals eksternal yang menghasilkan ekspansi tulang rusuk.
Ini menyebabkan penurunan tekanan intrapleural, yang menyebabkan ekspansi paru-paru yang menghasilkan peningkatan volume paru-paru. Oleh karena itu, tekanan intrapulmoner berkurang sesuai dengan apa yang dinyatakan dalam hukum Boyle-Mariotte.
Ketika tekanan intrapulmoner adalah subatmosferik, udara atmosfer mengalir ke paru-paru, menghasilkan peningkatan tekanan di paru-paru; menyamakan, tekanannya terhadap tekanan atmosfer, dan menyimpulkan fase inspirasi.
Selanjutnya, otot-otot inspirasi rileks dan otot-otot ekspirasi berkontraksi. Selain itu, terjadi retraksi elastis paru, sebuah fenomena yang menghasilkan penurunan volume paru-paru, dengan konsekuensi peningkatan tekanan intrapulmoner, yang dapat dijelaskan oleh hukum Boyle-Mariotte..
Dengan meningkatkan tekanan intrapulmoner, dan menjadi lebih besar dari tekanan atmosfer, udara mengalir dari bagian dalam paru-paru ke atmosfer. Ini terjadi sampai tekanan disamakan, yang mengakhiri fase kedaluwarsa.
Contoh (percobaan)
Eksperimen 1
Balon kecil ditempatkan tertutup rapat, membuat simpul di mulutnya, di dalam jarum suntik, tempat plunger telah dilepas, sekitar 20 ml. Plunger jarum suntik ditempatkan di bagian tengah jarum suntik, jarum dilepas dan saluran udara terhalang..
Pengamatan
Dengan perlahan-lahan menarik plunger dari injektor, teramati bahwa balon mengembang.
Penjelasan
Dua tekanan diberikan pada dinding balon: tekanan pada wajah bagian dalamnya, produk dari udara yang terkandung di dalam balon, dan tekanan lain pada permukaan luar balon, diberikan oleh udara yang terkandung dalam jarum suntik.
Saat menarik plunger dari injektor, setengah vakum dibuat di dalamnya. Oleh karena itu, tekanan udara di permukaan luar dinding pompa berkurang, membuat tekanan yang diberikan di dalam pompa relatif lebih besar..
Tekanan bersih ini, menurut hukum Boyle-Mariote, akan menghasilkan distensi dinding balon dan peningkatan volume balon.
Eksperimen 2
Potong botol plastik, kira-kira setengahnya, pastikan potongannya sejajar mungkin. Di mulut botol, sebuah balon yang disesuaikan ditempatkan, pada saat yang sama sejumlah air ditempatkan dalam piring yang dalam.
Pengamatan
Dengan menempatkan bagian bawah botol dengan balon di atas air piring, balon itu cukup mengembang.
Penjelasan
Air menggeser sejumlah udara tertentu, meningkatkan tekanan udara pada dinding botol dan bagian dalam balon. Ini menyebabkan, menurut hukum Boyle-Mariotte, peningkatan volume dunia, yang divisualisasikan oleh inflasi dunia.
Referensi
- Wikipedia. (2019). Hukum Boyle. Diperoleh dari: en.wikipedia.org
- Redaksi Encyclopaedia Britannica. (27 Juli 2018). Hukum Boyle. Encyclopædia Britannica. Diperoleh dari: britannica.com
- Helmenstine, Todd. (5 Desember 2018). Formula untuk Hukum Boyle. Diperoleh dari: thoughtco.com
- Film-film India Muda. (15 Mei 2018). Hukum Boyle: Eksperimen Sains Untuk Anak-Anak. Diperoleh dari: yifindia.com
- Cecilia Bembibre (22 Mei 2011). Balon udara panas Definisi ABC. Diperoleh dari: definicionabc.com
- Ganong, W, F. (2003). Fisiologi Medis (Edisi ke-19). Editorial Manual Modern.


