Hibridisasi Kimia sp, sp2, sp3
itu hibridisasi kimia adalah "campuran" orbital atom, yang konsepnya diperkenalkan oleh ahli kimia Linus Pauling pada tahun 1931 untuk menutupi ketidaksempurnaan Teori Link Valencia (TEV). Ketidaksempurnaan apa? Ini adalah: geometri molekul dan panjang tautan ekivalen dalam molekul seperti metana (CH4).
Menurut TEV, dalam metana orbital atom C membentuk empat ikatan σ dengan empat atom H. Orbital 2p dengan bentuk formas (gambar bawah) C saling tegak lurus satu sama lain, sehingga Hs harus dipisahkan. orang lain pada sudut 90º.
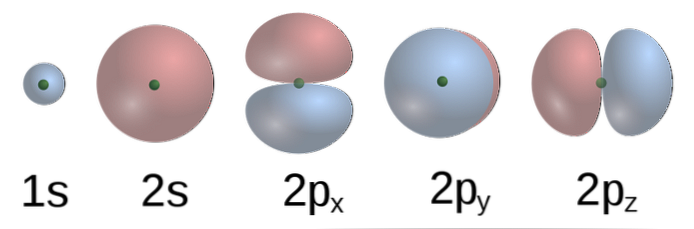
Selain itu, orbital 2s (berbentuk bola) dari C dikaitkan dengan orbital 1s dari H pada sudut 135º sehubungan dengan tiga Hs lainnya. Namun, secara eksperimental telah ditemukan bahwa sudut dalam CH4 adalah 109,5 º dan bahwa, di samping itu, panjang ikatan C-H adalah setara.
Untuk menjelaskan hal ini, kombinasi orbital atom asli harus dipertimbangkan untuk membentuk empat orbital hibrid yang terdegenerasi (dengan energi yang sama). Di sinilah kimia kimia. Seperti apa orbital hibrid? Itu tergantung pada orbital atom yang menghasilkannya. Mereka juga menunjukkan campuran karakteristik elektronik ini.
Indeks
- 1 sp3 Hibridisasi
- 1.1 Interpretasi
- 1.2 Penyimpangan sudut tautan
- 2 Hibridisasi sp2
- 3 Hibridisasi sp
- 4 Referensi
Hibridisasi sp3
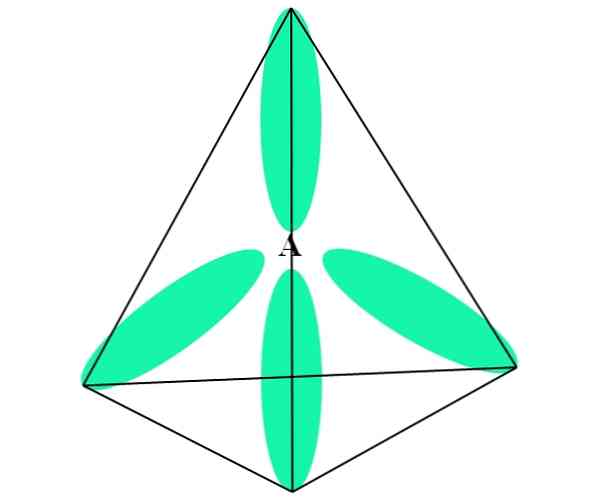
Dalam kasus CH4, Hibridisasi C adalah sp3. Dari pendekatan ini, geometri molekul dijelaskan dengan empat orbital sp3 dipisahkan pada 109,5º dan menunjuk ke arah simpul tetrahedron.
Pada gambar di atas Anda dapat melihat bagaimana orbital sp3 (hijau) membangun lingkungan elektronik tetrahedral di sekitar atom (A, yang merupakan C untuk CH4).
Mengapa 109,5º dan bukan sudut lain, untuk "menggambar" geometri yang berbeda? Alasannya adalah bahwa sudut ini meminimalkan tolakan elektronik dari empat atom yang terhubung ke A.
Dengan cara ini, molekul CH4 dapat direpresentasikan sebagai tetrahedron (geometri molekul tetrahedral).
Jika, alih-alih H, C membentuk hubungan dengan kelompok atom lain, apa yang kemudian akan menjadi hibridisasi? Selama karbon membentuk empat ikatan σ (C-A), hibridisasinya akan3.
Dapat diasumsikan bahwa dalam senyawa organik lainnya seperti CH3OH, CCl4, C (CH3)4, C6H12 (sikloheksana), dll., karbon memiliki hibridisasi sp3.
Ini merupakan hal mendasar untuk membuat sketsa struktur organik, di mana karbon dengan ikatan sederhana merupakan titik divergensi; artinya, struktur tidak tetap dalam satu bidang tunggal.
Interpretasi
Apa interpretasi paling sederhana untuk orbital hibrida ini tanpa membahas aspek matematis (fungsi gelombang)? Orbital sp3 menyiratkan bahwa mereka berasal oleh empat orbital: satu dan tiga p.
Karena kombinasi orbital atom ini dianggap ideal, orbital empat sp3 dihasilkan adalah identik dan menempati orientasi yang berbeda di ruang angkasa (seperti dalam orbital px, haldan dan halz).
Hal di atas berlaku untuk sisa hibridisasi yang mungkin terjadi: jumlah orbital hibrid yang terbentuk sama dengan orbital atom gabungan. Misalnya, orbital hibrid sp3d2 mereka terbentuk dari enam orbital atom: satu s, tiga p dan dua d.
Penyimpangan sudut tautan
Menurut Teori Penolakan Pasangan Elektronik dari Lapisan Valencia (VSEPR), sepasang elektron bebas menempati lebih banyak volume daripada atom yang terhubung. Hal ini menyebabkan tautan terpisah, mengurangi tegangan elektronik dan mengalihkan sudut 109,5º:
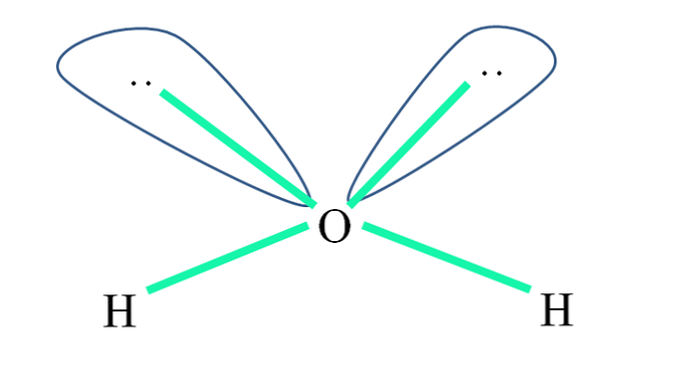
Sebagai contoh, dalam molekul air, atom H terikat pada orbital sp3 (berwarna hijau), dan juga pasangan elektron yang tidak dibagi ":" menempati orbital ini.
Repulsi pasangan elektron ini biasanya direpresentasikan sebagai "dua bola dengan mata", yang, karena volumenya, mengusir kedua ikatan σ O-H.
Jadi, di dalam air, sudut-sudut tautan benar-benar 105º, bukannya 109,5º yang diharapkan untuk geometri tetrahedral.
Geometri apa yang dimiliki H?2O? Ini memiliki geometri sudut. Mengapa Karena meskipun geometri elektronik adalah tetrahedral, dua pasang elektron yang tidak dibagi mengurangi ke geometri molekul sudut.
Hibridisasi sp2
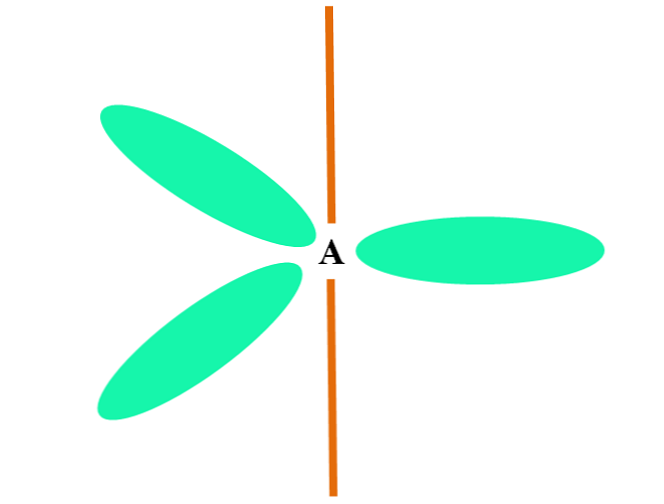
Ketika sebuah atom menggabungkan dua orbital p dan satu, ia menghasilkan tiga orbital hibrid sp2; Namun, p orbital tetap tidak berubah (karena mereka bertiga), yang direpresentasikan sebagai bilah oranye pada gambar di atas.
Di sini, tiga orbital sp2 mereka berwarna hijau untuk menyoroti perbedaan mereka dari bilah oranye: orbital "murni".
Atom dengan hibridisasi sp2 dapat divisualisasikan sebagai lantai trigonal datar (segitiga yang digambar dengan orbital sp2 warna hijau), dengan simpul-simpulnya dipisahkan oleh sudut 120º dan tegak lurus terhadap batang.
Dan apa peran yang dimainkan orbital murni? Itu membentuk ikatan rangkap (=). Orbital sp2 memungkinkan pembentukan tiga ikatan σ, sedangkan orbital p murni ikatan π (ikatan rangkap dua atau rangkap tiga menyiratkan satu atau dua ikatan π).
Misalnya, untuk menggambar gugus karbonil dan struktur molekul formaldehida (H2C = O), hasil sebagai berikut:
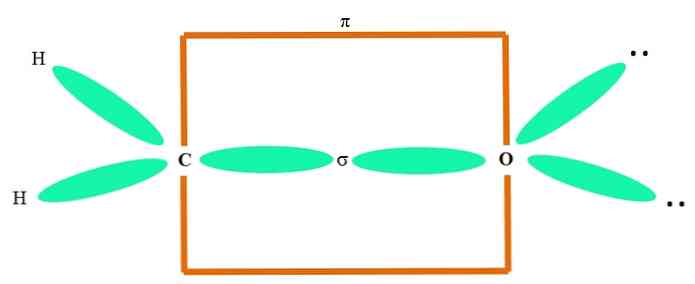
Orbital sp2 baik C dan O membentuk ikatan σ, sedangkan orbital murni mereka membentuk ikatan π (persegi oranye).
Dapat dilihat bagaimana sisa gugus elektronik (atom H dan pasangan elektron yang tidak digunakan bersama) terletak di orbital sp lainnya.2, dipisahkan oleh 120º.
Hibridisasi sp
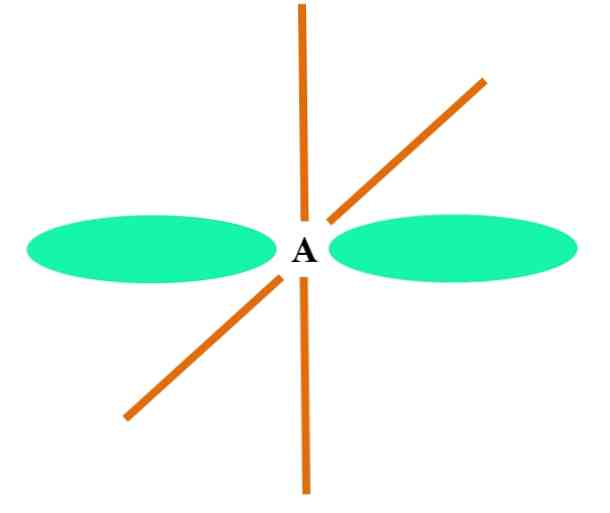
Gambar atas menunjukkan atom A dengan hibridisasi sp. Di sini, orbital s dan p orbital bergabung untuk menghasilkan dua orbital sp terdegenerasi. Namun, sekarang dua orbital p murni tidak berubah, yang memungkinkan A untuk membentuk dua ikatan rangkap atau ikatan rangkap tiga (≡).
Dengan kata lain: jika dalam struktur a C sesuai dengan yang di atas (= C = atau C≡C), maka hibridasinya adalah sp. Untuk atom yang kurang ilustratif lainnya - seperti logam transisi - deskripsi geometri elektronik dan molekul rumit karena orbital d dan bahkan orbital f juga dipertimbangkan..
Orbital hibrida dipisahkan oleh sudut 180º. Untuk alasan ini, atom-atom yang terhubung diatur dalam geometri molekul linier (B-A-B). Akhirnya, pada gambar di bawah ini Anda dapat melihat struktur anion sianida:

Referensi
- Sven. (3 Juni 2006). S-p-Orbit. [Gambar] Diperoleh pada 24 Mei 2018, dari: commons.wikimedia.org
- Richard C. Banks. (Mei 2002). Ikatan dan Hibridisasi. Diperoleh pada 24 Mei 2018, dari: chemistry.boisestate.edu
- James (2018). Pintasan Hibridisasi. Diperoleh pada 24 Mei 2018, dari: masterorganicchemistry.com
- Ian Hunt. Departemen Kimia, Universitas Calgary. hibridisasi sp3. Diperoleh pada 24 Mei 2018, dari: chem.ucalgary.ca
- Ikatan Kimia II: Geometri Molekuler dan Hibridisasi Orbit Atom Bab 10. [PDF]. Diperoleh pada 24 Mei 2018, dari: wou.edu
- Quimitube (2015). Ikatan kovalen: Pengantar hibridisasi orbital atom. Diperoleh pada 24 Mei 2018, dari: quimitube.com
- Menggigil & Atkins. (2008). Kimia anorganik (Edisi keempat, halaman 51). Mc Graw Hill.


