Sejarah kalorimeter, bagian, tipe dan karakteristiknya
itu kalorimeter adalah alat yang digunakan untuk mengukur perubahan suhu dari jumlah zat (biasanya air) dari panas spesifik yang diketahui. Perubahan suhu ini disebabkan oleh panas yang diserap atau dilepaskan dalam proses yang sedang dipelajari; kimia jika merupakan reaksi, atau fisik jika terdiri dari fase atau keadaan berubah.
Di laboratorium, kalorimeter paling sederhana yang dapat ditemukan adalah cangkir kopi. Ini digunakan untuk mengukur panas yang diserap atau dilepaskan dalam reaksi pada tekanan konstan, dalam larutan air. Reaksi dipilih untuk menghindari intervensi reagen atau produk gas.
 Dalam reaksi eksotermik, jumlah panas yang dilepaskan dapat dihitung dari peningkatan suhu kalorimeter dan larutan encer:
Dalam reaksi eksotermik, jumlah panas yang dilepaskan dapat dihitung dari peningkatan suhu kalorimeter dan larutan encer:
Jumlah panas yang dilepaskan dalam reaksi = jumlah panas yang diserap oleh kalorimeter + jumlah panas yang diserap oleh larutan
Jumlah panas yang diserap oleh kalorimeter disebut kapasitas kalor kalorimeter. Ini ditentukan dengan memasok sejumlah panas yang diketahui ke kalorimeter dengan massa air tertentu. Kemudian, peningkatan suhu kalorimeter dan larutan yang dikandungnya diukur.
Dengan data ini, dan penggunaan panas spesifik air (4,18 J / g.ºC), kapasitas kalori kalorimeter dapat dihitung. Kapasitas ini juga disebut konstanta kalorimeter.
Di sisi lain, panas yang diperoleh oleh larutan berair sama dengan m · ce · Δt. Dalam rumus m = massa air, ce = panas air spesifik dan Δt = variasi suhu. Mengetahui semua ini, seseorang kemudian dapat menghitung jumlah panas yang dilepaskan oleh reaksi eksotermik.
Indeks
- 1 Sejarah kalorimeter
- 2 Bagian
- 3 Jenis dan karakteristiknya
- 3.1 Cangkir kopi
- 3.2 Pompa kalorimetri
- 3.3 Kalorimeter adiabatik
- 3.4 Kalorimeter isoperibolik
- 3.5 Aliran kalorimeter
- 3.6 Kalorimeter untuk kalorimetri pemindaian diferensial
- 4 Aplikasi
- 4.1 Secara fisikokimia
- 4.2 Dalam sistem biologis
- 4.3 Kalorimeter pompa oksigen dan daya kalori
- 5 Referensi
Sejarah kalorimeter
Pada tahun 1780, A. L. Lavoisier, ahli kimia Perancis, yang dianggap sebagai salah satu bapak kimia, menggunakan kelinci percobaan untuk mengukur produksi panas melalui pernapasannya..
Bagaimana? Menggunakan perangkat yang mirip dengan kalorimeter. Panas yang dihasilkan oleh kelinci percobaan dibuktikan dengan mencairnya salju yang mengelilingi peralatan.
Peneliti A. L Lavoisier (1743-1794) dan P. S. Laplace (1749-1827) merancang kalorimeter yang digunakan untuk mengukur panas spesifik suatu benda dengan metode pencairan es.
Kalorimeter terdiri dari gelas silinder berlapis timah, dipernis, dipegang oleh tripod dan diakhiri secara internal dengan corong. Di dalam, gelas lain ditempatkan, mirip dengan yang sebelumnya, dengan tabung yang melewati ruang luar dan yang dilengkapi dengan kunci. Di dalam gelas kedua ada kotak.
Dalam kisi-kisi ini ditempatkan makhluk atau objek yang spesifik panasnya ingin ditentukan. Es ditempatkan di dalam bejana konsentris, seperti di keranjang.
Panas yang dihasilkan oleh tubuh diserap oleh es, menyebabkan fusi. Dan produk air cair dari pencairan es dikumpulkan, membuka kunci kaca bagian dalam.
Dan akhirnya, menimbang air, massa es cair itu diketahui.
Bagian
Kalorimeter yang paling umum digunakan di laboratorium pengajaran kimia adalah apa yang disebut kalorimeter cangkir kopi. Kalorimeter ini terdiri dari gelas kimia, atau wadah dari bahan anime yang memiliki sifat isolasi tertentu. Di dalam wadah ini solusi air ditempatkan dengan tubuh yang akan menghasilkan atau menyerap panas.
Di bagian atas wadah penutup bahan isolasi dengan dua lubang ditempatkan. Dalam satu termometer diperkenalkan untuk mengukur perubahan suhu, dan yang lain pengaduk, lebih disukai dari bahan gelas, yang melakukan fungsi memindahkan isi larutan berair..
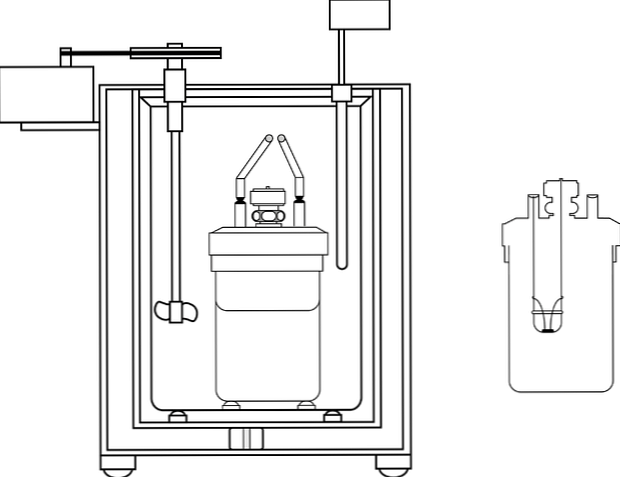
Gambar menunjukkan bagian-bagian dari pompa kalorimetri; Namun, dapat diamati bahwa ia memiliki termometer dan agitator, elemen umum dalam beberapa kalorimeter.
Jenis dan karakteristiknya
Cangkir kopi
Ini adalah salah satu yang digunakan dalam penentuan panas yang dilepaskan oleh reaksi eksotermik, dan panas yang diserap dalam reaksi endotermik.
Selain itu, dapat digunakan dalam menentukan panas spesifik tubuh; yaitu, jumlah panas yang perlu diserap satu gram zat untuk menaikkan suhunya satu derajat Celcius. .
Pompa kalorimetri
Ini adalah perangkat di mana jumlah panas yang dilepaskan atau diserap dalam suatu reaksi yang terjadi pada volume konstan diukur.
Reaksi berlangsung di kapal baja yang kuat (pompa), yang direndam dalam volume air yang besar. Ini membuat perubahan suhu air kecil. Oleh karena itu, diasumsikan bahwa perubahan yang terkait dengan reaksi diukur pada suhu dan volume konstan.
Di atas menunjukkan bahwa tidak ada pekerjaan yang dilakukan ketika reaksi dilakukan dalam pompa kalorimetri.
Reaksi dimulai dengan memasok listrik melalui kabel yang terhubung ke pompa.
Kalorimeter adiabatik
Ini ditandai dengan memiliki struktur isolasi yang disebut perisai. Perisai terletak di sekitar sel tempat perubahan suhu dan panas terjadi. Ini juga terhubung ke sistem elektronik yang menjaga suhunya sangat dekat dengan sel, untuk menghindari perpindahan panas.
Dalam kalorimeter adiabatik, perbedaan suhu antara kalorimeter dan sekitarnya diminimalkan; serta meminimalkan koefisien perpindahan panas dan waktu untuk pertukaran panas.
Bagian-bagiannya terdiri dari:
-Sel (atau wadah), diintegrasikan ke dalam sistem insulasi yang dengannya ia mencoba untuk menghindari kehilangan panas.
-Termometer, untuk mengukur perubahan suhu.
-Pemanas, terhubung ke sumber tegangan listrik yang dapat dikendalikan.
-Dan perisai, sudah disebutkan.
Dalam jenis kalorimeter ini, sifat-sifat seperti entropi, suhu Debye dan densitas keadaan elektronik dapat ditentukan.
Kalorimeter isoperibolik
Ini adalah perangkat di mana sel reaksi dan pompa direndam dalam struktur yang disebut jaket. Dalam hal ini, jaket yang disebut terdiri dari air, dijaga pada suhu konstan.
Suhu sel dan pompa meningkat ketika panas dilepaskan selama proses pembakaran; tetapi suhu jaket air dipertahankan pada suhu yang tetap.
Mikroprosesor mengontrol suhu sel dan jaket, membuat koreksi yang diperlukan dari panas bocor yang dihasilkan dari perbedaan antara dua suhu.
Koreksi ini diterapkan terus menerus, dan dengan koreksi akhir, berdasarkan pengukuran sebelum dan sesudah pengujian.
Kalorimeter aliran
Dikembangkan oleh Caliendar, ia memiliki perangkat untuk memindahkan gas dalam sebuah wadah dengan kecepatan konstan. Saat menambahkan panas, peningkatan suhu dalam cairan diukur.
Kalorimeter aliran ditandai dengan:
- Pengukuran yang tepat dari laju aliran konstan.
- Pengukuran akurat jumlah panas yang dimasukkan ke dalam cairan melalui pemanas.
- Pengukuran akurat kenaikan suhu dalam gas yang disebabkan oleh input energi
- Desain untuk mengukur kapasitas gas di bawah tekanan.
Kalorimeter untuk kalorimetri pemindaian diferensial
Ini ditandai dengan memiliki dua wadah: dalam satu sampel untuk dipelajari ditempatkan, sementara yang lain disimpan kosong atau bahan referensi digunakan.
Kedua kapal dipanaskan dengan kecepatan energi konstan, dengan menggunakan dua pemanas independen. Ketika pemanasan kedua wadah dimulai, komputer akan membuat grafik perbedaan aliran panas dari pemanas terhadap suhu, sehingga mampu menentukan aliran panas.
Selain itu, variasi suhu sebagai fungsi waktu dapat ditentukan; dan akhirnya, kapasitas kalori.
Aplikasi
Secara fisikokimia
-Kalorimeter dasar, jenis cangkir kopi, memungkinkan untuk mengukur jumlah panas yang dikeluarkan atau diserap tubuh. Mereka dapat menentukan apakah suatu reaksi eksotermik atau endotermik. Selain itu, panas spesifik suatu benda dapat ditentukan.
-Dengan kalorimeter adiabatik telah dimungkinkan untuk menentukan entropi dari suatu proses kimia dan kepadatan elektronik dari negara..
Dalam sistem biologis
-Mikrokalorimeter digunakan untuk mempelajari sistem biologis yang mencakup interaksi antar molekul, serta perubahan konformasi molekuler yang terjadi; misalnya, dalam terungkapnya suatu molekul. Jalur ini mencakup pemindaian diferensial dan titrasi isotermal.
-Mikrokalorimeter digunakan dalam pengembangan obat-obatan molekul kecil, bioterapi, dan vaksin.
Kalorimeter pompa oksigen dan daya kalori
Pembakaran berbagai zat terjadi dalam kalorimeter pompa oksigen, dan kekuatan kalorinya dapat ditentukan. Di antara zat yang dipelajari melalui penggunaan kalorimeter ini adalah: batubara dan kokas; minyak nabati, baik yang berat maupun yang ringan; bensin dan semua bahan bakar motor.
Serta jenis bahan bakar untuk reaktor pesawat; limbah bahan bakar dan pembuangan limbah; produk makanan dan suplemen untuk nutrisi manusia; hijauan tanaman dan suplemen untuk pakan ternak; bahan bangunan; bahan bakar roket dan propelan.
Demikian juga, kekuatan kalori telah ditentukan oleh kalorimetri dalam studi termodinamika bahan yang mudah terbakar; dalam studi keseimbangan energi dalam ekologi; dalam bahan peledak dan bubuk termal dan dalam pengajaran metode termodinamika dasar.
Referensi
- Whitten, Davis, Peck & Stanley. Kimia (Edisi ke-8). CENGAGE Learning.
- González J., Cortés L. & Sánchez A. (s.f.). Kalorimetri adiabatik dan aplikasinya. Dipulihkan dari: cenam.mx
- Wikipedia. (2018). Kalorimeter. Diperoleh dari: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22 Juni 2018). Definisi Kalorimeter dalam Kimia. Diperoleh dari: thoughtco.com
- Gillespie, Claire. (11 April 2018). Bagaimana cara kerja kalorimeter? Ilmu pengetahuan. Diperoleh dari: sciencing.com


