Sifat Karakteristik Materi (Fisik dan Kimia)
itu sifat karakteristik materi mereka adalah sifat kimia atau fisik yang dapat membantu mengidentifikasi atau membedakan satu zat dari yang lain. Sifat fisik adalah karakteristik suatu zat yang diamati dengan indera. Sifat kimia adalah karakteristik yang menggambarkan bagaimana suatu zat berubah dari satu zat ke zat lain selama reaksi kimia.
Beberapa sifat fisik suatu zat adalah kerapatan, kelarutan, titik leleh, warna dan massa. Sifat kimiawi bahan tersebut meliputi sifat mudah terbakar, reaktivitas dengan asam dan korosi. Beberapa contoh tentang bagaimana sifat-sifat materi dapat membantu mengidentifikasi suatu unsur adalah dengan membandingkan kepadatan berbagai unsur.
Unsur seperti emas memiliki kerapatan 19,3 gram per sentimeter kubik sedangkan kerapatan belerang adalah 1,96 gram per sentimeter kubik. Demikian pula, titik leleh zat seperti air dan isopropil alkohol berbeda.
Sifat fisik materi
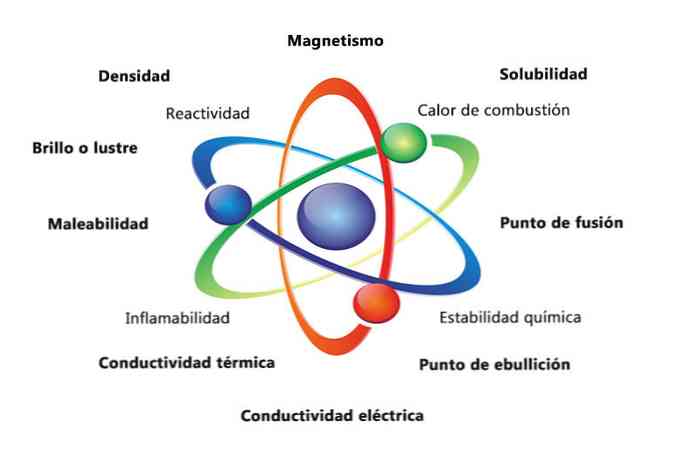
Sifat fisik materi adalah sifat yang dapat diukur atau diamati tanpa mengubah sifat kimia zat tersebut. Beberapa contoh sifat fisik adalah:
- Kepadatan: jumlah materi yang memiliki objek, dihitung dengan membagi massa berdasarkan volume.
- Magnetisme: kekuatan tarik-menarik antara magnet dan objek magnetik.
- Kelarutan: mengukur seberapa baik suatu zat dapat larut dalam zat lain.
- Titik lebur: suhu di mana suatu zat berubah dari padat menjadi cair.
- Titik didih: suhu di mana suatu zat berubah dari cair menjadi gas.
- Konduktivitas listrik: adalah ukuran seberapa baik arus listrik bergerak melalui suatu zat.
- Konduktivitas termal: kecepatan perpindahan suatu zat.
- Kelenturan: adalah kemampuan suatu zat untuk digulung atau digiling dengan berbagai cara.
- Gloss atau kilau: adalah seberapa mudah objek memantulkan cahaya.
Sifat kimia dari materi
Sifat kimia menggambarkan kemampuan suatu zat untuk mengubah dirinya menjadi zat baru dengan sifat yang berbeda. Di bawah ini adalah beberapa contoh sifat kimia:
- Panas pembakaran: adalah energi yang dilepaskan ketika suatu senyawa mengalami pembakaran sempurna dengan oksigen.
- Stabilitas kimia: mengacu pada apakah suatu senyawa akan bereaksi dengan air atau udara (zat yang stabil secara kimia tidak akan bereaksi).
- Kemudahan terbakar: kemampuan suatu senyawa untuk terbakar ketika terkena nyala api.
- Reaktivitas: kemampuan untuk berinteraksi dengan zat lain dan membentuk satu atau lebih zat baru.
Keadaan fisik materi
Materi adalah segala sesuatu yang menempati ruang, yang memiliki massa dan yang dapat dirasakan oleh indera kita. Materi dapat diklasifikasikan menurut kondisi fisiknya: padat, cair dan gas.
1- Padatan dan sifat karakteristiknya
Semua padatan memiliki massa, menempati ruang, memiliki volume dan bentuk yang ditentukan, tidak melewati ruang dan tidak dapat dikompresi atau memiliki bentuk yang kaku. Sebagai contoh, kayu, buku, spons, logam, batu, dll..
Dalam benda padat, partikel-partikel kecil materi sangat berdekatan dan saling bersentuhan. Partikel-partikel itu begitu berdekatan sehingga mereka tidak bisa bergerak banyak, ada sangat sedikit ruang di antara mereka.
2- Cairan dan sifat karakteristiknya
Semua cairan memiliki massa, menempati ruang, memiliki volume yang ditentukan tetapi bukan bentuk yang ditentukan (karena mereka beradaptasi dengan wadah di mana mereka berada), mereka dapat dikompresi ke tingkat yang sangat kecil dan dapat meluncur melalui ruang. Sebagai contoh yang kita miliki: air, minyak tanah, minyak, dll..
Dalam cairan, partikel kecil materi sedikit lebih jauh dari satu sama lain, ada lebih banyak ruang di antara mereka (dibandingkan dengan padatan) dan mereka tidak saling bersentuhan. Oleh karena itu, partikel dapat bergerak di antara ruang, mendorong dan bertabrakan dengan partikel lain, terus berubah arah.
3- Gas dan sifat karakteristiknya
Semua gas memiliki massa, menempati ruang, tidak memiliki volume atau bentuk yang ditentukan, dapat dikompresi dengan sangat luas dan dapat berdifusi ke ruang angkasa. Sebagai contoh yang kita miliki: hidrogen, oksigen, nitrogen, karbon dioksida, uap, dll..
Dalam gas, partikel-partikel kecil materi terpisah jauh lebih jauh, ada lebih banyak ruang di antara mereka (dibandingkan dengan cairan) dan mereka tidak saling bersentuhan. Partikel-partikel memiliki kebebasan bergerak maksimum sehingga mereka mendorong dan bertabrakan dengan partikel lain yang terus berubah arah.
Perubahan keadaan materi
Materi dapat dikonversi dari keadaan padat ke keadaan cair dan sebaliknya, dan dari keadaan cair ke keadaan gas dan sebaliknya. Konversi ini mengambil nama perubahan kondisi materi dan terjadi oleh perubahan suhu:
Fusion
Perubahan keadaan material dari padat menjadi cair dengan cara peningkatan suhu. Ketika zat padat dipanaskan, panas menyebabkan partikel bergetar lebih kuat.
Setelah mencapai titik leleh, partikel padat memiliki energi kinetik yang cukup untuk mengatasi gaya tarik energi yang menahan mereka dalam posisi tetap, dan mereka pecah untuk membentuk kelompok kecil partikel cair..
Mendidih atau penguapan
Perubahan keadaan zat cair menjadi gas melalui peningkatan suhu. Ketika zat cair dipanaskan, panas membuat partikel bergerak lebih cepat.
Setelah mencapai titik didih, partikel cair memiliki energi kinetik yang cukup untuk mengatasi gaya tarik yang menahan mereka dalam posisi tetap, dan terpisah menjadi partikel gas individu..
Pembekuan atau pemadatan
Perubahan keadaan zat cair menjadi padat dengan cara penurunan suhu. Ketika zat cair didinginkan, partikel-partikelnya kehilangan banyak energi kinetik. Ketika mencapai titik beku, partikel berhenti bergerak dan bergetar dalam posisi tetap menjadi partikel padat.
Pencairan atau kondensasi
Perubahan keadaan materi gas menjadi cair dengan cara penurunan suhu. Ketika zat gas didinginkan, partikelnya kehilangan banyak energi kinetik yang menyebabkan mereka menarik satu sama lain menjadi partikel cair.
Sublimasi
Beberapa bahan berubah langsung dari bentuk padatnya ke bentuk gas atau sebaliknya, tanpa melalui kondisi cair. Ketika zat padat ini dipanaskan, partikelnya bergerak sangat cepat sehingga terpisah sepenuhnya membentuk uap atau gas, dan sebaliknya ketika proses terjadi dari gas ke zat padat.
Referensi
- De Podesta, M. Memahami sifat-sifat materi, edisi ke-2. Inggris Raya: Taylor & Francis.
- Goel A. Kondisi materi. New Delhi: Rumah Penerbitan Discovery.
- Moore J, Stanitski C. Ilmu molekuler, edisi ke-5. Stamford: Cengage Learning.
- Ramakrishna A. Sifat materi, edisi pertama. New Delhi: Goyal Brothers Prakashan.
- Reger D, Goode S, Ball D. Chemistry. Prinsip dan praktik, edisi ke-3. Kanada: Brooks / Cole, Cengage Learning.
- Shapere D. Matter (fisika). Diperoleh dari: accessscience.com.
- Singh L, Kaur M. Hal di lingkungan kita. India: Sekolah S. Chand.


