Karakteristik Trypanosoma brucei, morfologi, siklus biologis, gejala
Trypanosoma brucei Ini adalah protozoa parasit ekstraseluler. Milik kelas Kinetoplastidae, genus Trypanosomatidae Trypanosoma. Ada dua subspesies yang menyebabkan dua varian berbeda trypanosomiasis manusia Afrika atau juga disebut "penyakit tidur".
Trypanosoma brucei subsp. gambiense, menyebabkan bentuk kronis dan 98% kasus, terletak di bagian barat dan tengah Afrika Sub-Sahara. Trypanosoma brucei subsp. Rhodesian adalah penyebab bentuk akut, hadir di tengah dan timur Afrika sub-Sahara.
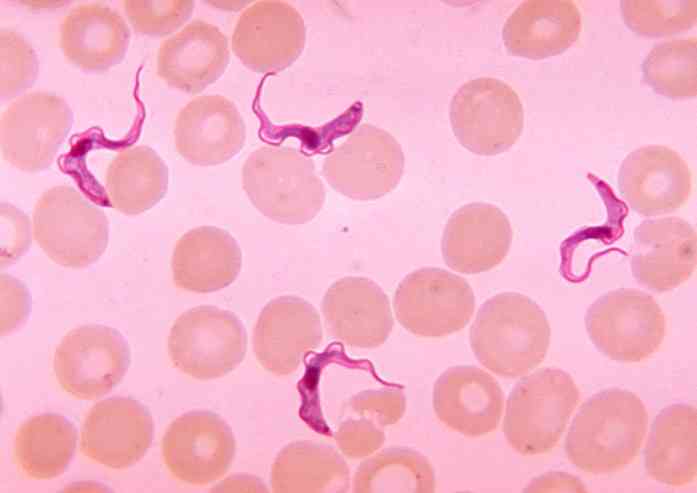
Kedua varian penyakit ini telah dilaporkan di negara-negara Afrika sub-Sahara di mana lalat tsetse ditemukan, Glossina spp, vektor atau agen pengirim dari T. brucei.
Subspesies ketiga, Trypanosoma brucei subsp. brucei, menyebabkan penyakit serupa pada hewan peliharaan dan liar, yang disebut nagana.
"Penyakit tidur" mengancam lebih dari 60 juta orang di 36 negara di Afrika sub-Sahara. Ada sekitar 300.000 hingga 500.000 kasus per tahun, di mana sekitar 70.000 hingga 100.000 meninggal. Infestasi oleh lalat tsetse mencakup wilayah 10 juta kilometer persegi, sepertiga dari daratan Afrika.
Organisasi Kesehatan Dunia mengakui penurunan yang signifikan dalam jumlah kasus baru trypanosomiasis manusia Afrika dalam beberapa tahun terakhir. Hal ini disebabkan oleh masih adanya inisiatif nasional dan internasional untuk mengendalikan penyakit ini.
Indeks
- 1 Karakteristik umum
- 1.1 Penemuan
- 1.2 Genetika
- 1.3 "Penyakit tidur" dan pemanasan global
- 2 Filogeni dan taksonomi
- 3 Morfologi
- 3.1 Formulir Tryomastigote
- 3.2 formulir epimastigote
- 3.3 Kinetosom
- 4 siklus biologis
- 4.1 Di inang (manusia atau mamalia lain)
- 4.2 Dalam lalat tsetse (vektor)
- 5 Gejala infeksi
- 5.1 Fase pertama
- 5.2 Fase kedua
- 5.3 Diagnosis
- 6 Perawatan
- 7 Referensi
Karakteristik umum
Ini disebut "penyakit tidur" karena menyebabkan pembalikan siklus tidur alami pasien. Orang tersebut tidur di siang hari dan tetap terjaga di malam hari. Ini adalah produk dari serangkaian gangguan psikis dan neurologis yang disebabkan oleh penyakit pada fase lanjutnya.
Penemuan
Hewan atau nagana trypanosomiasis adalah penyakit penting pada sapi di Afrika. Dia mengidentifikasi dirinya sendiri Trypanosoma brucei sebagai agen penyebab pada tahun 1899. Itu adalah David Bruce saat menyelidiki wabah besar Nagana di Zululand.
Belakangan, Aldo Castellani mengidentifikasi spesies trypanosome ini dalam darah dan cairan serebrospinal pasien manusia dengan "penyakit tidur".
Antara 1902 dan 1910, dua varian penyakit pada manusia dan subspesies penyebabnya diidentifikasi. Baik hewan dan manusia dapat bertindak sebagai reservoir parasit yang mampu menyebabkan penyakit pada manusia.
Genetika
Genom dari inti Trypanosoma brucei itu terdiri dari 11 kromosom diploid dan seratus kromosom mikro. Secara total memiliki 9.068 gen. Genom mitokondria (kinetoplast) terdiri dari banyak salinan DNA sirkular.
"Penyakit tidur" dan pemanasan global
Trypanosomiasis manusia Afrika dianggap sebagai salah satu dari 12 penyakit menular manusia yang dapat diperburuk oleh pemanasan global.
Ini disebabkan oleh kenyataan bahwa ketika suhu sekitar meningkat, area yang rentan ditempati oleh lalat akan diperbesar. Glossina sp. Saat menjajah teritori baru, ia akan membawa parasit itu.
Filogeni dan taksonomi
Trypanosoma brucei pmilik kerajaan Protista, grup Excavata, filum Euglenozoa, kelas Kinetoplastidae, urutan Trypanosomatida, keluarga Trypanosomatidae, genus Trypanosoma, subgenre Trypanozoon.
Spesies ini memiliki tiga subspesies yang menyebabkan berbagai varian "penyakit tidur" pada manusia (T. b. subsp. gambiense dan T. b. subsp. rHodesian) dan pada hewan peliharaan dan liar (T. b. subsp. brucei).
Morfologi
Formulir Tripomastigote
Trypanosoma brucei adalah organisme uniseluler memanjang dengan panjang 20 μm dan lebar 1-3 μm, yang bentuk, struktur, dan komposisi membrannya bervariasi sepanjang siklus hidupnya.
Ini memiliki dua bentuk dasar. Bentuk tripomastigote tubuh basal posterior ke nukleus dan flagel panjang. Formulir ini pada gilirannya mengasumsikan subtipe selama siklus hidup. Dari jumlah tersebut, subtipe pendek atau gemuk (lesu dalam bahasa Inggris), lebih tebal dan flagelnya pendek.
Bentuk epimastigote
Bentuk dasar kedua adalah epimastigote tubuh basal anterior ke nukleus dan flagel agak lebih pendek dari yang sebelumnya.
Sel ditutupi oleh lapisan glikoprotein permukaan variabel. Lapisan ini mengubah glikoprotein dari permukaannya dan dengan demikian menghindari serangan antibodi yang dihasilkan oleh inang.
Sistem kekebalan menghasilkan antibodi baru untuk menyerang konfigurasi baru lapisan dan perubahan lapisan lagi. Inilah yang disebut variasi antigenik.
Kinetosoma
Fitur penting adalah keberadaan kinetosoma. Struktur ini terdiri dari DNA mitokondria terkondensasi yang terletak di dalam mitokondria satu-satunya yang ada. Mitokondria besar ini terletak di dasar momok.
Siklus biologis
Siklus hidup Trypanosoma brucei bergantian antara lalat tsetse sebagai vektor dan manusia sebagai tuan rumah. Untuk berkembang di host yang berbeda seperti itu, protozoon mengalami perubahan metabolisme dan morfologis yang penting dari satu ke yang lain.
Dengan cepat, Trypanosoma brucei mendiami saluran pencernaan, sedangkan pada manusia ia ditemukan dalam darah.
Di inang (manusia atau mamalia lainnya)
Trypanosoma brucei Ia datang dalam tiga bentuk dasar sepanjang siklusnya. Ketika lalat menggigit manusia atau mamalia lain untuk mengekstraksi darahnya, ia menyuntikkan dari kelenjar ludahnya ke dalam aliran darah bentuk nonproliferatif dari protozoa, yang disebut metacyclic.
Begitu berada dalam aliran darah, itu berubah menjadi bentuk proliferatif, yang disebut darah ramping (ramping dalam Bahasa Inggris).
Bentuk darah ramping Trypanosoma brucei ia mendapat energinya dari glikolisis glukosa yang ada dalam darah. Proses metabolisme ini dilakukan dalam organel yang disebut glikosoma. Trypanosom ini berkembang biak dalam cairan tubuh yang berbeda: darah, getah bening dan cairan serebrospinal.
Ketika jumlah parasit dalam darah meningkat, mereka mulai berubah lagi menjadi bentuk non-proliferasi. Kali ini adalah varian yang lebih tebal dengan flagel yang lebih pendek, yang disebut darah montok (kekar).
Tripanosom darah tuberous disesuaikan dengan kondisi sistem pencernaan lalat. Mereka mengaktifkan mitokondria dan enzim yang diperlukan untuk siklus asam sitrat dan rantai pernapasan. Sumber energi bukan lagi glukosa tetapi prolin.
In the fly tse-tsé (vektor)
Vektor atau agen transmisi dari Trypanosoma brucei itu adalah tse-tse fly, Glossina spp. Genus ini mengelompokkan 25 hingga 30 spesies lalat hematophagous. Mereka mudah dibedakan dari lalat biasa dengan bekantan yang panjang dan sayap terlipat penuh saat istirahat.
Ketika lalat tsetse menggigit mamalia inang yang terinfeksi dan mengekstraksi darah, bentuk darah pendek ini menembus vektor.
Setelah berada di saluran pencernaan lalat, darah yang gemuk terbentuk dengan cepat berdiferensiasi menjadi tripanosom proliferatif proklik.
Mereka berkembang biak dengan pembelahan biner. Mereka meninggalkan saluran pencernaan lalat dan pergi ke kelenjar ludah. Mereka ditransformasikan menjadi epimastigotes yang berlabuh ke dinding oleh momok.
Di kelenjar liur, mereka berkembang biak dan berubah menjadi trypanosomes metacyclic, siap untuk diinokulasi lagi ke dalam sistem darah mamalia.
Gejala infeksi
Masa inkubasi penyakit ini adalah 2 hingga 3 hari setelah gigitan lalat. Gejala neurologis dapat terjadi setelah beberapa bulan dalam kasus T. b. subsp. gambiense. Jika ini tentang T. b. subsp. Rhodesian, mungkin butuh bertahun-tahun untuk mewujudkannya.
Fase pertama
"Penyakit tidur" memiliki dua tahap. Yang pertama disebut tahap awal atau fase hemolimfatik, ditandai dengan adanya Trypanosoma brucei hanya di dalam darah dan getah bening.
Dalam kasus ini, gejalanya adalah demam, sakit kepala, nyeri otot, muntah, pembengkakan kelenjar getah bening, penurunan berat badan, kelemahan dan sifat mudah marah..
Pada fase ini penyakitnya bisa dikacaukan dengan malaria.
Fase kedua
Yang disebut tahap akhir atau fase neurologis (keadaan ensefalitis), diaktifkan dengan kedatangan parasit di sistem saraf pusat, yang terdeteksi dalam cairan serebro-spinal. Di sini gejalanya diekspresikan sebagai perubahan perilaku, kebingungan, inkoordinasi, perubahan siklus tidur dan akhirnya koma.
Perkembangan penyakit berlanjut dengan siklus hingga tiga tahun dalam kasus subspesies gambiense, berakhir dengan kematian. Ketika subspesies hadir Rhodesian, kematian datang dari minggu ke bulan.
Dari kasus-kasus yang tidak mengalami perawatan, 100% meninggal. 2-8% dari kasus yang diobati juga mati.
Diagnosis
Tahap diagnostik adalah ketika bentuk infektif, yaitu trypanosome darah, ditemukan dalam darah.
Melalui pemeriksaan mikroskopis sampel darah, bentuk spesifik dari parasit terdeteksi. Pada fase ensefalitis diperlukan pungsi lumbal untuk menganalisis cairan serebrospinal.
Ada beberapa teknik molekuler untuk mendiagnosis keberadaan Trypanosoma brucei.
Perawatan
Kapasitas yang dimiliki Trypanosoma brucei terus memvariasikan konfigurasi lapisan luar glikoproteinnya (variasi antigenik), membuatnya sangat sulit untuk mengembangkan vaksin melawan "penyakit tidur".
Tidak ada kemoterapi profilaksis dan sedikit atau tidak ada prospek vaksin. Empat obat utama yang digunakan untuk trypanosomiasis Afrika manusia beracun.
Melarsoprol adalah satu-satunya obat yang efektif untuk kedua varian penyakit sistem saraf pusat. Namun, sangat beracun sehingga membunuh 5% pasien yang menerimanya.
Eflornithine, sendiri atau dalam kombinasi dengan nifurtimox, semakin digunakan sebagai terapi lini pertama untuk penyakit yang disebabkan oleh Trypanosoma brucei subsp. gambiense.
Referensi
- Fenn K dan KR Matthews (2007) Biologi sel diferensiasi Trypanosoma brucei. Opini Saat Ini dalam Mikrobiologi. 10: 539-546.
- Fernández-Moya SM (2013) Karakterisasi fungsional protein pengikat RNA RBP33 dan DRBD3 sebagai regulator ekspresi gen Trypanosoma brucei. TESIS DOKTORAL INI. Institut Parasitologi dan Biomedis "López-Neyra". Universitas Editorial Granada, Spanyol. 189 hal.
- García-Salcedo JA, D Pérez-Morga, P Gijón, V Dilbeck, E Pays dan DP Nolan (2004) Peran diferensial untuk aktin selama siklus hidup Trypanosoma brucei. The EMBO Journal 23: 780-789.
- Kennedy PGE (2008) Masalah berlanjut dari manusia trypanosomiasis Afrika (penyakit tidur). Annals of Neurology, 64 (2), 116-126.
- Matthews KR (2005) Biologi sel perkembangan dari Trypanosoma brucei. J. Cell Sci. 118: 283-290.
- Welburn SC, EM Fèvre, PG Coleman, M Odiit dan I Maudlin (2001) Penyakit tidur: kisah dua penyakit. TREND dalam Parasitologi. 17 (1): 19-24.


